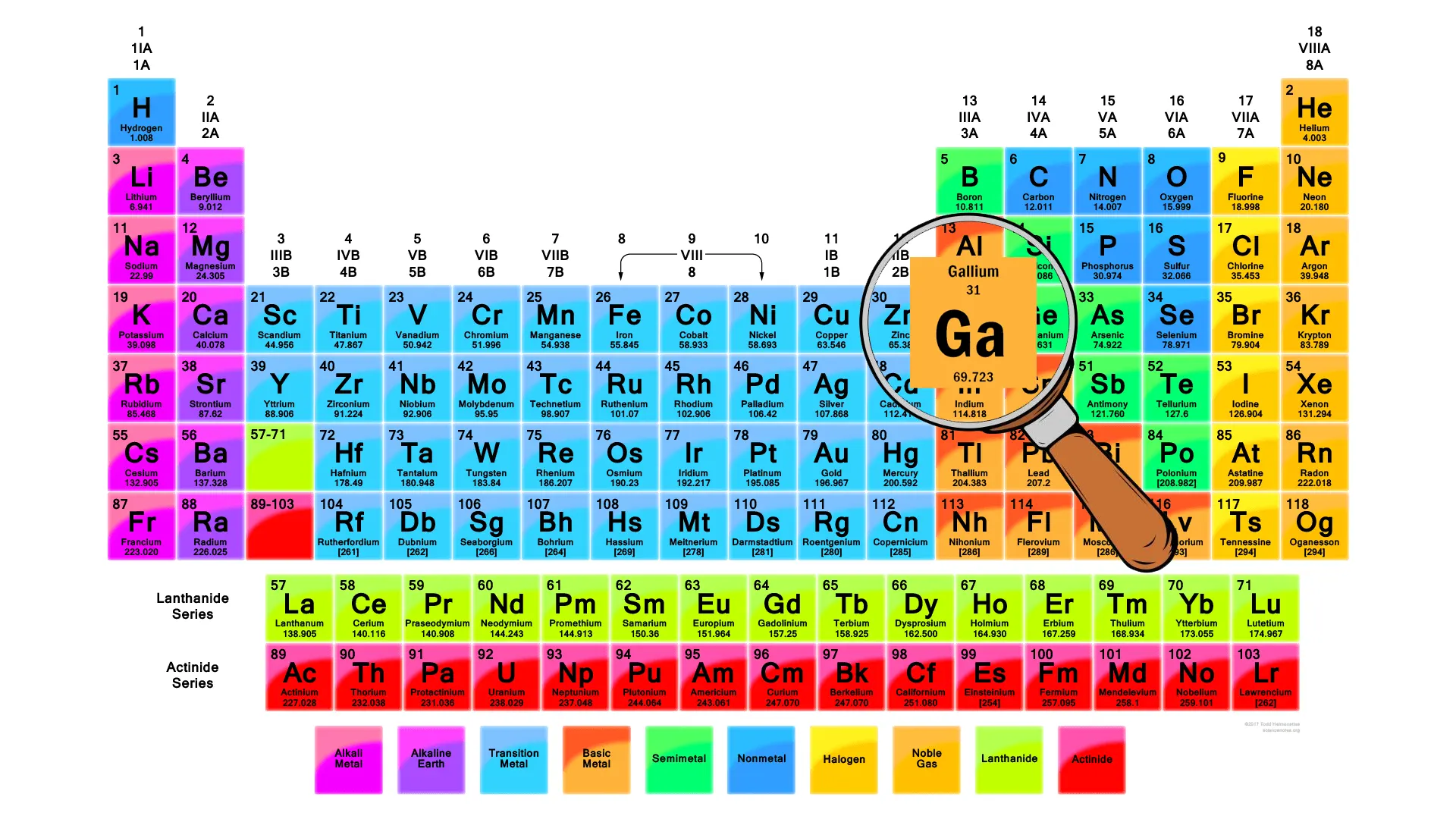
فلزات، یک گروه از عناصر شیمیایی هستند که خواص فیزیکی و شیمیایی خاصی دارند. این خواص شامل مثلاً رسانایی حرارت و الکتریسیته، خواص مغناطیسی، قابلیت انعطاف و سختی و دمای ذوب میشوند. فلزات به دو دسته فلزات سبک (مانند آلومینیوم و آهن) و فلزات سنگین (مانند جیوه و طلا) تقسیم میشوند. یکی از فلزات جالب و جذاب در جدول تناوبی عنصرها، گالیوم است. گالیوم فلزی نرم و سفید است که در دمای اتاق به صورت جامد و در دماهای بالاتر به صورت مایع وجود دارد. این فلز برای استفاده در صنایع الکترونیک، نورپردازی، آینهسازی و به عنوان یک عنصر آلیاژی مورد استفاده قرار میگیرد. همچنین، گالیوم نقش مهمی در فناوری نیمهرساناها و لیزرها نیز دارد. حال که به اهمیت این فلز شگفتانگیز پی بردید، در ادامه با صباپروفیل همراه باشید تا به بررسی بیشتر آن بپردازیم.
فهرست مطالب
گالیوم چیست؟
گالیوم (به انگلیسی Gallium) عنصری شیمیایی با نماد Ga و عدد اتمی 31 است. این عنصر در جدول تناوبی قرار گرفته و به گروه بورون از عناصر فلزی سبک تعلق دارد. گالیوم در دمای اتاق به صورت جامد و سفید رنگ است، اما در دماهای بالاتر از حدود 29.76 درجه سانتیگراد به صورت مایع تبدیل میشود. این ویژگی باعث میشود که گالیوم به عنوان یکی از عناصری با دمای ذوب پایین قابل استفاده در مجاورت دماهای بالا باشد.
گالیوم خواصی شبیه به آلومینیوم دارد و مانند آن، خواص رسانایی حرارت و الکتریسیته قابل توجهی دارد. همچنین، گالیوم مقاومت خوبی در برابر خوردگی دارد. به دلیل این ویژگیها، گالیوم در صنایع مختلفی استفاده میشود. برای مثال، در صنایع الکترونیک، به عنوان جزء ساختمانی در تراشههای نیمهرساناها و دیودها استفاده میشود. همچنین، در تولید آینههای خاص و نورپردازی، گالیوم به عنوان یک رنگدهنده و فیلتر استفاده میشود.
گالیوم به صورت طبیعی به صورت سنگ وجود ندارد، به عنوان یک فلز نادر در زمینهٔ کانیشناسی دیده نمیشود. به طور معمول، گالیوم به صورت ترکیبات خاص در معادن دیگر وجود دارد. گالیوم بیشتر در کانیهایی مانند سفالزیت (GaPO4), آلمانیت (CuGaS2), و زینکیت (ZnGa2O4) یافت میشود. اما در طبیعت به صورت مستقیم و خالص سنگ گالیوم وجود ندارد.
علاوه بر آن، گالیوم به صورت تخلخل در کانیهای برخی از سنگهای معدنی دیگر نیز یافت میشود، اما به طور معمول از این کانیها برای استخراج گالیوم به صورت صنعتی استفاده نمیشود. استخراج گالیوم به صورت صنعتی عمدتاً از کانی بوکسیت (Bauxite) که در فرایند استخراج آلومینیوم استفاده میشود، صورت میگیرد. گالیوم به صورت آلایش در بوکسیت وجود داشته و از طریق فرآیندهای پالایش آلومینیوم استخراج میشود.
بنابراین، گالیوم به صورت سنگ طبیعی در طبیعت یافت نمیشود و بیشتر به صورت ترکیبات در کانیها یا به صورت آلایش در سایر معدنی استخراج میشود.
مشخصات عنصر گالیوم
گالیم (با نماد شیمیایی Ga و عدد اتمی 31) یک عنصر شیمیایی در جدول تناوبی است. در زیر مشخصات بیشتری از عنصر گالیم را میتوانید بیابید:
| علامت اختصاری | Ga |
| عدد اتمی | 31 |
| وزن اتمی (گرم بر مول) | 69.723 |
| نقطه ذوب (درجه سانتیگراد) | 29.78 |
| نقطه جوش (درجه سانتیگراد) | 2,403 |
| گروه | 13 |
| دوره | 4 |
| نوع عنصر | فلز |
| شماره CAS | 7440-55-3 |
| ساختار الکترونی | [Ar] 3d10 4s2 4p1 |
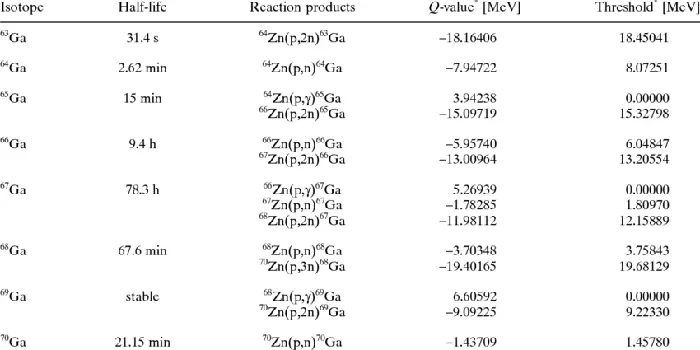
ایزوتوپ های گالیوم
گالیم سه ایزوتوپ پایدار دارد که عبارتند از:
1. گالیم-69 (Ga-69): این ایزوتوپ دارای 31 پروتون و 38 نوترون است. ایزوتوپ Ga-69 یکی از ایزوتوپهای نسبتاً فراوان گالیم است و حدود 60.11٪ از عنصر گالیم را تشکیل میدهد. این ایزوتوپ بهطور گستردهای در علم و صنعت استفاده میشود. همچنین، Ga-69 میتواند به عنوان یک شاخص در برخی تحقیقات علمی و کاربردهای پزشکی (مانند تصویربرداری هستهای) نیز بهکار رود.
2. گالیم-71 (Ga-71): دارای 31 پروتون و 40 نوترون است. Ga-71 نیز بهصورت طبیعی در گالیم وجود دارد، اما نسبت فراوانی نسبت به Ga-69 کمتر است. حدود 39.89٪ از عنصر گالیم را ایجاد میکند. این ایزوتوپ همچنین در تحقیقات علمی و کاربردهای صنعتی و پزشکی مورد استفاده قرار میگیرد.
3. گالیم-72 (Ga-72): ایزوتوپ Ga-72 دارای 31 پروتون و 41 نوترون است. این ایزوتوپ کمتر فراوانی در گالیم طبیعی دارد و نسبتی بسیار کمتر از آن را تشکیل میدهد. با این حال، Ga-72 همچنان در تحقیقات علمی و برخی کاربردهای خاص مورد استفاده قرار میگیرد.
هر کدام از این ایزوتوپها تعداد پروتون و الکترون یکسانی دارند و تنها در تعداد نوترونهای خود تفاوت دارند. ایزوتوپهای گالیم از لحاظ خواص شیمیایی واکنشها، به طور کلی مشابه هستند، اما به دلیل تفاوت در جرم هستهای، ممکن است در برخی واکنشها و کاربردها تفاوت نمایان شوند.
ایزوتوپهای گالیم، علاوه بر کاربردهای صنعتی، در دامپزشکی، تحقیقات هستهای، و فیزیک هستهای نیز کاربرد دارند. همچنین، گالیم خواصی متفاوت از برخی عناصر دیگر دارد و میتواند در ترکیب با دیگر عناصر بهعنوان کاتد فعال در برخی باتریها و نیز در ساخت فلزات آلیاژی استفاده شود.
گالیوم ۶۸ چیست؟
گالیوم به عنوان دارو در تکنیکهای تصویربرداری پزشکی استفاده میشود. گالیوم-۶۸ یک نوع ایزوتوپ از عنصر گالیوم است که با عدد جرمی ۶۸ و نماد Ga-68 نشان داده میشود. ایزوتوپها نسخههایی از یک عنصر هستند که تعدادی پروتون و نوترون مشخص دارند و میتوانند در تجزیهپذیری و کاربردهای مختلف مورد استفاده قرار بگیرند.
گالیوم-۶۸ به صورت یک رادیوایزوتوپ مصنوعی است که از گالیوم-۶۹ با استفاده از فرآیند تجزیهپذیری تولید میشود. این ایزوتوپ از نظر پرتوزایی بسیار مناسب است و در پزشکی هستهای استفاده میشود. مهمترین کاربرد گالیوم-۶۸ در تصویربرداری مولکولی با استفاده از تکنیک پوزیترون اشعهای (PET) است.
در تصویربرداری مولکولی با استفاده از گالیوم-۶۸، یک ترکیب شیمیایی به نام گالیوم-۶۸ دوفلوئورو-دوکسوگلوزوز (Ga-68 DOTATOC) استفاده میشود. این ترکیب قادر است به تشخیص و تصویربرداری بیماریهایی مانند تومورهای نورواندوکراین و بعضی از سایر تومورهای سلولهای بتا در سیستم عصبی مرکزی و جسم سلولهای متعدد در بدن کمک کند.
به عنوان مثال، در تصویربرداری PET-CT با استفاده از گالیوم-۶۸، میتوان با تزریق ترکیب Ga-68 DOTATOC، تومورهای نورواندوکراین را در بدن تصویربرداری کرده و موقعیت و اندازه آنها را به دقت تشخیص داد.
تکنولوژی PET با استفاده از گالیوم-۶۸ و سایر رادیوایزوتوپها، امکان تشخیص و پیگیری بیماریها و بررسی فعالیتهای مولکولی در بدن را فراهم میکند.
عوارض اسکن گالیوم
استفاده از رادیوایزوتوپ گالیوم-۶۸ در اسکن پوزیترون اشعهای (PET) برای تصویربرداری مولکولی معمولاً ایمن است و عوارض جدی ندارد. گالیوم-۶۸ دارای عمر نیمهعمر کوتاهی است و بعد از چند ساعت (حدود ۶۸ دقیقه) تجزیه میشود. این به این معنی است که دوز اشعهای که بیمار دریافت میکند، بسیار کم و محدود به زمان اسکن میباشد. با این حال، همانند هر فرآیند پزشکی دیگر، ممکن است عوارض واکنشهای ناخواسته و ناراحتیهای کمی در اثر استفاده از رادیوایزوتوپ گالیوم-۶۸ در اسکن پوزیترون اشعهای رخ دهد. برخی از عوارض ممکن عبارتند از:
۱. واکنشهای حساسیتی: برخی از بیماران ممکن است به رادیوفارماسوتیکال حاوی گالیوم-۶۸ حساسیت نشان دهند و واکنشهای حساسیتی مانند آلرژی را تجربه کنند. این واکنشها معمولاً خفیف هستند و میتوان با تجویز داروهای ضدحساسیت درمان شوند.
۲. اثرات جانبی موضعی: ممکن است بعد از تزریق رادیوفارماسوتیکال، در محل تزریق درد، التهاب، یا سوزش احساس شود. این عوارض موضعی معمولاً طی چند ساعت بعد از اسکن بهبود مییابند.
۳. عوارض متابولیک: بعضی از بیماران ممکن است عوارض متابولیکی ناشی از تزریق رادیوایزوتوپ گالیوم-۶۸ مانند تغییر در سطح آنزیمها را تجربه کنند.
خواص عنصر گالیوم
گالیوم خواص فیزیکی و شیمیایی منحصر به فردی دارد که در زیر توضیح داده شده است:
1. نقطه ذوب پایین: گالیوم یک فلز با نقطه ذوب بسیار پایین است و در حدود 29.8 درجه سانتیگراد ذوب میشود. این ویژگی باعث میشود که گالیوم در دماهای معمولی به صورت جامد باقی بماند.
2. خاصیت فلزی: گالیوم یک فلز است و خواص فلزی از جمله رسانایی الکتریکی و حرارتی را داراست. این فلز در دمای اتاق نیز مقاومت الکتریکی نسبتاً بالایی دارد.
3. قابلیت تغییر شکل: گالیوم از خواص مهم دیگری برخوردار است از جمله اینکه قابلیت تغییر شکل را به خوبی دارد. به عنوان مثال، در دمای اتاق میتوان آن را با انگشتان خم کرد.
4. مقاومت شیمیایی: گالیوم مقاومت خوبی در برابر بسیاری از اسیدها و قلیایها دارد. اما در برابر اسیدهای قوی مانند اسید نیتریک غلیظ و هیدروکلریک غلیظ حل میشود.
5. استفادههای فناورانه: به دلیل خواص خاصی که دارد، گالیوم در صنایع نوظهور نیز استفادههای زیادی دارد. برخی از کاربردهای گالیوم شامل ساختن فوتوسلهها، مدارهای الکترونیکی با سرعت بالا، لامپهای الکتریکی، ترانزیستورهای بیسیم و تولید نیروی الکتریکی در سلولهای خورشیدی است.
تاریخچه گالیوم
تاریخچه گالیم یا گالیوم به طور معمول با کشف آن توسط عالم فرانسوی به نام پل-امیل لکو د بویسباودران (Paul-Émile Lecoq de Boisbaudran) آغاز شد. پل امیل را که در سال 1838 متولد شد، به عنوان کاشف عناصر گالیوم (1875)، ساماریوم (1880) و دیسپروزیم (1886) شناخته میشود.

در سال 1875، کاشف گالیوم، پل امیل به طور تصادفی گالیم را در یک نمونه از زیرکونیت گیاهی کشف کرد. او با تجزیه نمونه زیرکونیت، موفق به جداسازی عنصر گالیم شد. نام گالیم از کلمهٔ لاتین “Gallia” گرفته شده است که به معنی “فرانسه” است، و اشاره به کشور محل کشف گالیم توسط او دارد. بعد از کشف گالیم، خواص آن بررسی شد و به طور متداول در تحقیقات علمی مورد استفاده قرار گرفت. در دههٔ 1880، روشهای بهتری برای تولید گالیم بهوجود آمد و استفاده از آن در صنعت نیز گسترش یافت.
امروزه، گالیم در بسیاری از صنایع و کاربردها مورد استفاده قرار میگیرد، از جمله الکترونیک، صنایع نورپردازی، باتریها، لیزرها، تصویربرداری هستهای، و فناوریهای نوین مرتبط با نانومواد.
بعد از کشف گالیم در سال 1875، عملیات استخراج و تولید این عنصر محدود بود. در اوایل تولید، گالیم توسط ذوب کردن خاک معدنی که حاوی گالیوم بود، بهدست میآمد. اما استخراج گالیوم با این روش مشکلاتی ایجاد میکرد، زیرا نیاز به دمای بالا برای ذوب داشت و عملیات جداسازی پیچیدهای را میطلبید.
در دههٔ 1880، روشهای بهتری برای تولید گالیم پیشنهاد شد. اما روشهای بهتری نیز برای تولید گالیوم از خاک معدنی مانند سولفید گالیم در دههٔ 1890 توسعه یافت. در اواخر قرن نوزدهم و اوایل قرن بیستم، استفاده از گالیم در بسیاری از صنایع رشد یافت. از جمله کاربردهای اولیه گالیوم میتوان به تولید آینههای نقرهای با روکش گالیم، استفاده در فیلترها و منابع نوری، استفاده در صنعت شیشه، تولید قلمهای نوری، و تحقیقات علمی در فیزیک و شیمی اشاره کرد.
در دههٔ 1960 و 1970، گالیوم در صنعت الکترونیک بهطور گستردهای استفاده شد. با توسعهٔ تکنولوژی نیمهرساناها، گالیوم و مرکبهای آن برای ساخت بخشهای الکترونیکی مورد استفاده قرار گرفتند. از آن زمان به بعد، کاربردهای گالیم در صنعت الکترونیک، نورپردازی، تکنولوژی نانو و صنایع پزشکی بهطور چشمگیری افزایش یافت.
از آن زمان تا به امروز، گالیم همچنان در صنایع مختلف مورد استفاده قرار میگیرد و با توسعهٔ فناوریهای جدید، کاربردهای جدیدتری برای این عنصر پیدا میشود.
کاربردهای گالیوم چیست؟
گالیوم در صنایع و کاربردهای مختلفی مورد استفاده قرار میگیرد. در زیر تعدادی از کاربردهای گالیوم را ذکر میکنیم:
1. الکترونیک: گالیوم به عنوان یک نیمهرسانای مهم در صنعت الکترونیک استفاده میشود. به خصوص در تراشههای نوری (optoelectronic) مانند دیودهای نوری (LED) و لیزرها، گالیوم به عنوان یک جزء اساسی استفاده میشود. این تراشهها در دستگاههای نمایش دیجیتال، روشنایی صفحه نمایشهای LED و لیزرهای نوری استفاده میشوند.
2. صنعت فضایی: به دلیل خواص فیزیکی و شیمیایی خاص خود، گالیوم در صنعت فضایی نیز کاربردهای متنوعی دارد. به عنوان مثال، گالیوم در تراشهها و سنسورهای فضایی استفاده میشود و قابلیت کار در شرایط دمایی بسیار پایین را دارد.
3. خمیر ترمز: یکی دیگر از کاربردهای گالیوم در صنعت خودروسازی استفاده از آن در خمیر ترمزهاست. خمیر ترمزی که گالیوم در آن حضور دارد، دارای خواصی است که باعث کاهش سایش و کاهش خوردگی بین قطعات ترمز میشود.
4. صنعت شیشه: گالیوم به عنوان یک عامل اصلاحکننده در صنعت شیشه استفاده میشود. افزودن گالیوم به شیشه میتواند خواص مکانیکی و نوری آن را بهبود بخشد.
5. پوششدهی سطح: گالیوم به صورت پوششدهی سطحی بر روی برخی از مواد استفاده میشود تا مقاومت به خوردگی و سایش را افزایش دهد.
6. تولید آلیاژها: گالیوم در تولید آلیاژها مانند آلیاژ گالینیوم-نیترید ارتباطی است که در صنعت فلزات و تولید تراشههای نیمهرسانایی مورد استفاده قرار میگیرد.
این تنها بخشی از کاربردهای گالیوم است و در برخی صنایع دیگر نیز ممکن است کاربردهای دیگری وجود داشته باشد.
معادن گالیوم در جهان
در زیر لیست مهمترین کشورهایی که دارای معادن عظیم گالیوم هستند را مشاهده مینمایید:
- چین: چین بزرگترین تولیدکننده گالیوم در جهان است و معادن گالیم در استانهای گوانگدونگ و جیانگکسی واقع شدهاند.
- استرالیا: استرالیا یکی از مهمترین تولیدکنندگان گالیوم است. معادن گالیوم در استانهای وسترن استرالیا و کوینزلند قرار دارند.
- روسیه: روسیه نیز تولیدکنندهٔ قابل توجهی از گالیوم است و معادن آن در مناطقی مانند سیبریا و اقلیم دالنی-ولنگا واقع شدهاند.
- کانادا: کانادا نیز منابع گالیم قابل توجهی دارد. معادن گالیم در استانهای منیتوبا و کیوبک قرار دارند.
- آمریکا: در ایالات متحده، معادن گالیوم در مناطقی مانند آلاسکا، جورجیا، وایومینگ و کلرادو قرار دارند.
علاوه بر این، معادن گالیم در برخی کشورهای دیگر نیز وجود دارد، از جمله آلمان، کره جنوبی، قزاقستان و بولیوی.
معادن گالیوم در ایران
منابع اولیه مهم گالیم در ایران شامل معدن بوکسیت جاجرم، زغال البرز شرقی و سرب روی انگوران است. نتایج نشان داده که گالیوم موجود در معدن بوکسیت جاجرم و فرآیند برگشتی بایر میتواند حائز اهمیت باشد. منابع ثانویه همواره از این حیث که دسترسی به آنها به دلیل عدم نیاز به هزینههای سرمایهگذاری جهت اکتشافات و استخراج ماده معدنی از اعماق زمین، همواره مورد توجه بودهاند. البته تاکنون هیچکدام از این معادن گفته شده، استخراج نشده است و تنها در حد تحقیقات اولیه بوده است.
قیمت گالیوم
قیمت جهانی گالیوم تحت تأثیر چند عامل قرار میگیرد. در زیر، برخی از عوامل تأثیرگذار بر قیمت گالیوم را ذکر میکنیم:
- عرضه و تقاضا: نسبت عرضه و تقاضا بر روی قیمت گالیوم تأثیر میگذارد. اگر تقاضا برای گالیوم افزایش یابد و عرضه آن کاهش یابد، قیمت ممکن است افزایش یابد. عکس العمل به تغییرات تقاضا در صنایع مختلف، به خصوص صنایع الکترونیک و نورپردازی، تأثیرگذار است.
- تولیدکنندگان اصلی: کشورهایی که تولیدکنندگان اصلی گالیوم هستند، میتوانند تأثیر مستقیمی بر قیمت داشته باشند. اگر تولیدکنندگان اصلی با مشکلاتی مانند کاهش تولید، محدودیتهای صادرات یا تغییرات قوانین و مقررات مواجه شوند، قیمت گالیوم ممکن است تحت تأثیر قرار بگیرد.
- مصرف در صنایع: صنایع مختلف از گالیوم برای کاربردهای مختلف استفاده میکنند. اگر صنایعی که به گالیوم نیاز دارند، رشد یا کاهش داشته باشند، این تغییرات میتوانند تأثیرگذار باشند. به عنوان مثال، افزایش استفاده از گالیوم در صنایع الکترونیک و نورپردازی در سالهای اخیر باعث افزایش قیمت آن شده است.
- سیاستهای دولتی: سیاستهای دولتی دربارهٔ صادرات، مالیات، تعرفهها و تنظیمات قوانین ممکن است بر قیمت گالیوم تأثیرگذار باشد. تغییرات در سیاستهای دولتی میتوانند قیمت گالیوم را تحت تأثیر قرار دهند.
- نرخ ارز: قیمت گالیوم معمولاً به دلار آمریکا برآورد میشود. در نتیجه، تغییرات نرخ ارز میتواند قیمت گالیوم را تحت تأثیر قرار دهد.
به طور کلی، قیمت گالیوم تحت تأثیر یک ترکیب از عوامل بازاری، اقتصادی و سیاسی قرار میگیرد و میتواند در طول زمان تغییر کند.
آلیاژهای گالیوم
گالیوم به صورت تک عنصری مورد استفاده قرار میگیرد، به عبارت دیگر به طور معمول با دیگر فلزات آلیاژ نمیشود. ولی در برخی موارد خاص، گالیوم با برخی فلزات آلیاژ تشکیل میدهد. در زیر تعدادی از آلیاژهای گالیوم را ذکر میکنم:
1. آلیاژ گالیم-آلومینیوم (Ga-Al): این آلیاژ شامل گالیوم و آلومینیوم است. این آلیاژ مقاومت مکانیکی بالا، مقاومت در برابر خوردگی و خواص حرارتی خوبی دارد. بنابراین در برخی صنایع مثل صنعت هوا و فضا، خودروسازی و صنایع مهندسی استفاده میشود.
2. آلیاژ گالیم-آنتیموان (Ga-Sb): این آلیاژ شامل گالیوم و آنتیموان است. این آلیاژ خواص نیمهرسانایی دارد و برای استفاده در تراشههای الکترونیکی، لیزرها و دستگاههای نوری مورد استفاده قرار میگیرد.
3. آلیاژ گالیم-نیترید (Ga-N): آلیاژ گالیوم-نیترید شامل گالیوم و نیتروژن است. این آلیاژ یک نیمهرسانای کاربردی است و در تراشههای الکترونیکی و الکترواپتیکی استفاده میشود.
4. آلیاژ گالیم-آرسنید (Ga-As): آلیاژ گالیوم-آرسنید یا آرسناید شامل گالیوم و آرسنیک است. این آلیاژ نیز به عنوان یک نیمهرسانا مهم در تراشههای الکترونیکی و اپتوالکترونیکی استفاده میشود.
این فقط بخشی از آلیاژهای گالیوم است و ممکن است آلیاژهای دیگری نیز وجود داشته باشند. ترکیبات و آلیاژهای گالیوم به دلیل خواص و کاربردهای منحصر به فرد خود، در برخی صنایع و فناوریها استفاده میشوند.
اکسید گالیوم چیست؟
گالیوم اکسید (Ga2O3) یا اکسید گالیوم، ترکیبی شیمیایی است که از گالیوم و اکسیژن تشکیل میشود. این ترکیب بخشی از خانوادهٔ ترکیبات گالیوم است و به صورت مادهٔ سفید یا بیرنگ یافت میشود. گالیوم اکسید به عنوان یک مادهٔ نیمهرسانا مورد توجه قرار گرفته است و کاربردهای متنوعی در صنعت الکترونیک و اپتوالکترونیک دارد. بعضی از کاربردهای گالیم اکسید عبارتند از:
- دیودهای نوری (LED)
- تراشههای تراستور قدرت (Power Transistors)
- دستگاههای نوری UV
- لیزرها
- تراشههای الکترونیکی
پرسش و پاسخ
عوارض مصرف گالیوم برای بدن چیست؟
در صورتی که گالیوم به صورت مستقیم مصرف شود یا به صورت غیرمستقیم وارد بدن شود، میتواند سمی باشد و عوارض جدی برای سلامتی ایجاد کند. گاهی اوقات از آن با نام بیماری گالیوم نیز نام میبرند. اما استفادههای استاندارد و معمول از گالیوم در تکنولوژی و صنایع به طور کلی ایمن و بدون خطر برای سلامتی است.
ترانزیستور گالیوم نیتراید چیست؟
ترانزیستور گالیوم نیتراید (GaN) یک نوع ترانزیستور نیمهرسانا است که از گالیوم نیترید (GaN) به عنوان مادهای فعال استفاده میکند. این ترانزیستورها در فناوری الکترونیک قدرت استفاده میشوند و به دلیل ویژگیهای برتر خود، جایگزین مناسبی برای ترانزیستورهای سیلیکونی به حساب میآیند. ترانزیستورهای گالیوم نیتراید از جمله ترانزیستورهای جریان بالا و ولتاژ بالا هستند که در ارتباطات بیسیم، سیستمهای رادار، تغذیه برق سوئیچینگ و سیستمهای نوری پیشرفته استفاده میشوند. ترانزیستورهای گالیوم نیتراید از نظر عملکرد و ویژگیهایشان از ترانزیستورهای سیلیکونی سنتی بهتر هستند و در بسیاری از صنایع الکترونیک قدرت و ارتباطات به صورت فزایندهای مورد استفاده قرار میگیرند.
گالیوم سولفات چیست؟
گالیم سولفات (با فرمول شیمیایی Ga2(SO4)3) یک ترکیب شیمیایی است که شامل گالیم و سولفات است. این ترکیب به صورت پودر سفید بیرنگی ظاهر میشود. در این ترکیب، گالیوم با اکسایش +3 و یون سولفات (SO4)2- به صورت گالیمیم سولفات گالیمیم (Ga3+) و یون سولفات (SO4)2- وابسته است. گالیوم سولفات در تحقیقات علمی و در برخی فرآیندهای شیمیایی و صنعتی استفاده میشود.
گالیم سیترات چیست؟
گالیم سیترات (با فرمول شیمیایی Ga(C6H5O7) یا Ga3C6H5O7) یک ترکیب شیمیایی است که شامل گالیم و سیترات است. سیترات نیز یک یون کمپلکسی است که از اسید سیتریک تشکیل میشود. گالیم سیترات به صورت پودر سفید بیرنگ یا کریستالهایی شفاف ظاهر میشود. گالیم سیترات به عنوان یک ترکیب آلیاژزایی استفاده میشود. در صنعت الکترونیک، این ترکیب به عنوان یک عامل پراکندگی و فیلم ساز استفاده میشود تا اتصالات الکتریکی روی سطوح مختلف بهبود یابد. همچنین، گالیم سیترات در برخی فرآیندهای کاتالیزوری نیز به عنوان عامل کاتالیزوری استفاده میشود. مهمترین کاربرد گالیم سیترات در پوششدهی فیلمهای نازک است. این فیلمها معمولاً بر روی سطوح مختلف اعم از فلزات، شیشه و سایر مواد آبدوست استفاده میشوند و میتوانند بهبود مقاومت الکتریکی، خازنسازی و خواص ضدخوردگی را فراهم کنند.
آیا گالیم شبه فلز است؟
خیر، گالیوم یک فلز است، نه یک شبه فلز.
هیدروکسید گالیوم چیست؟
هیدروکسید گالیوم (Ga(OH)3) ترکیب شیمیاییای است که شامل گالیم و یون هیدروکسید (OH-) میباشد. این ترکیب در شرایط آبی قابل تشکیل است و به صورت یک پودر سفید رنگ است. هیدروکسید گالیوم معمولاً به عنوان میانجی در تولید دیگر ترکیبات گالیوم، مانند گالیوم نیترات یا گالیوم اکسید، استفاده میشود. همچنین ممکن است در برخی فرآیندهای شیمیایی و صنعتی به عنوان کاتالیزور یا عامل اختلاط استفاده شود. مهمترین کاربرد هیدروکسید گالیوم در تهیه نانوذرات گالیوم اکسید است. این نانوذرات به عنوان مواد اولیه در ساخت انواع سلولهای خورشیدی، ترانزیستورهای نیمهرسانا و دیودهای گالیوم نیترید مورد استفاده قرار میگیرند.
فرق گالیوم و جیوه در چیست؟
گالیوم و جیوه به عنوان عناصر شیمیایی دارای خصوصیات و کاربردهای منحصر به فردی هستند و در صنعت الکترونیک و نیمهرساناها نقش مهمی ایفا میکنند. گالیوم (Ga) و جیوه (Ge) هر دو عناصر شیمیایی هستند، اما دارای خصوصیات و ویژگیهای مختلفی هستند.
1. خصوصیات فیزیکی:
– گالیوم: در دمای معمولی به شکل جامد در ظاهر نرم و نقرهای است و در دماهای بالاتر از 29.7 درجه سلسیوس به حالت مایع تبدیل میشود. دارای نقطه ذوب پایینی است.
– جیوه: در دمای معمولی به شکل جامد قرمز تیره است. جیوه دارای نقطه ذوب بالاتری نسبت به گالیوم است.
2. موقعیت در جدول تناوبی:
– گالیوم: در جدول تناوبی عنصری با عدد اتمی 31 و نماد Ga است. در گروه 13 قرار دارد.
– جیوه: در جدول تناوبی عنصری با عدد اتمی 32 و نماد Ge است. در گروه 14 قرار دارد.
3. کاربردها:
– گالیوم: گالیوم به دلیل خواص الکترونیکی خاص، در صنعت الکترونیک، ساخت و ساز، ساخت دیودها و برخی آلیاژها استفاده میشود.
– جیوه: جیوه به دلیل خواص نیمهرسانایی خود، در صنعت الکترونیک، ساخت ترانزیستورها، مدارهای مجتمع نوری و سلولهای خورشیدی مورد استفاده قرار میگیرد.
فلزات, مقالات در گروه صبا | نویسنده : امید مرادی | بروزرسانی : 17 آبان 1402