نیکل، فلزی همه کاره با خواص استثنایی، به دلیل ویژگیهای منحصر به فرد خود در صنایع مختلف مورد توجه قرار گرفته است. هدف این مقاله بررسی تقاضای فزاینده برای نیکل، برجسته کردن کاربردهای متنوع آن، روندهای فعلی بازار و چشماندازهای آینده است. با بررسی گسترش استفاده از نیکل در بخشهای کلیدی، خوانندگان میتوانند بینشهایی درباره عواملی که تقاضای نیکل را افزایش میدهند و فرصتهای بالقوهای که در پیش رو دارند به دست آورند. پس در ادامه با صباپروفیل همراه باشید.
فهرست مطالب
نیکل چیست؟
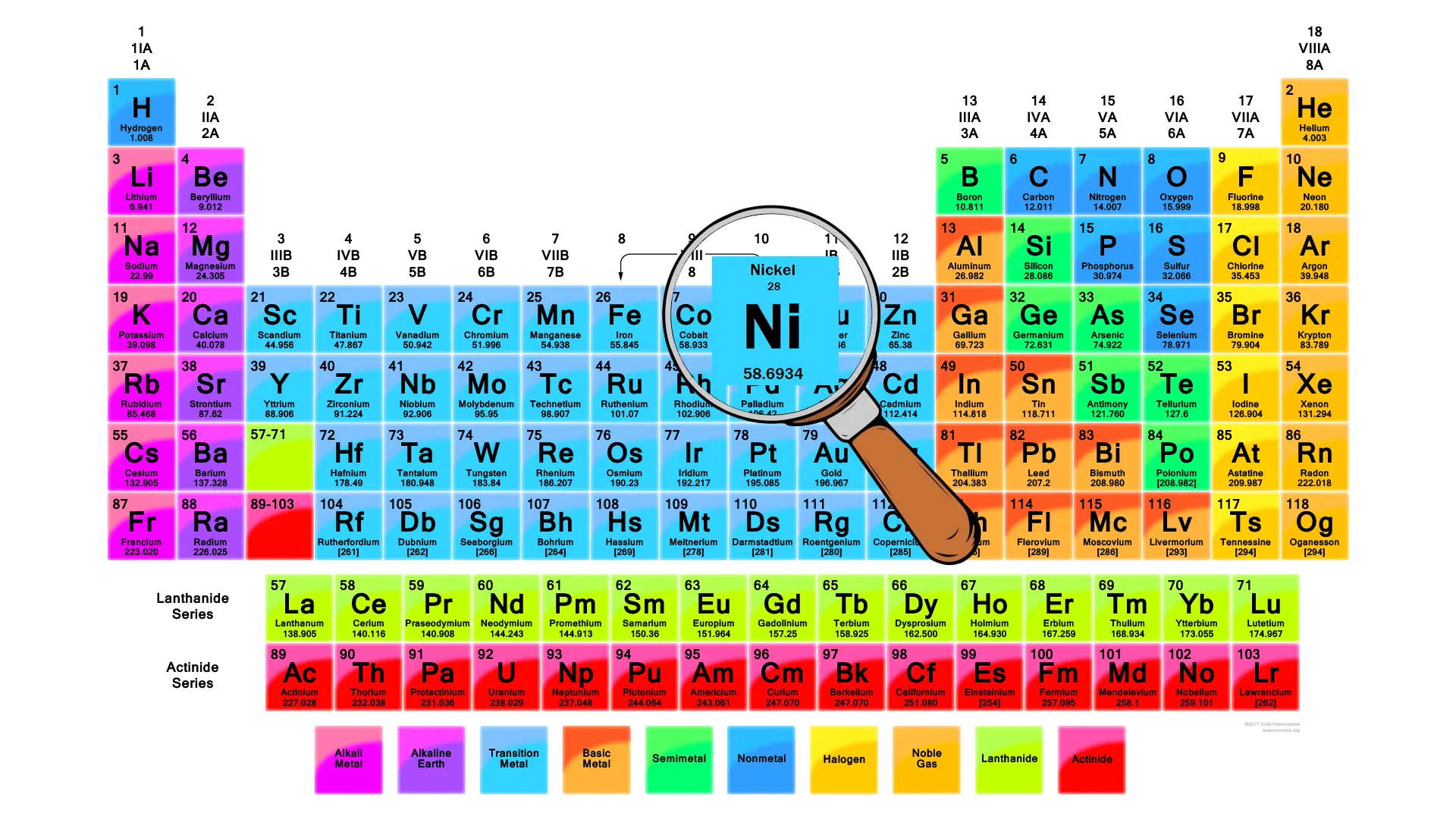
نیکل یک فلز واکنشپذیر، به رنگ نقرهای سفید و با بازتاب نور بالا است. این فلز در جدول تناوبی با نماد Ni و عدد اتمی 28 قرار دارد. نیکل یکی از فلزات انتقالی است و خواصی مانند مقاومت در برابر خوردگی و مقاومت مکانیکی بالا دارد و همچنین نقش مهمی در صنایع مختلف دارد.
نیکل یک عنصر فلزی است که بسیار مقاوم در برابر اکسیداسیون و خوردگی است. به عنوان یک فلز مقاوم، نیکل به طور گسترده در تولید فولاد ضد زنگ (استنلس استیل) استفاده میشود. نیکل میزان مقاومت و سختی فولاد را افزایش داده و خواص مقاومتی و زیبایی استنلس استیل را بهبود میبخشد.
علاوه بر استفاده در تولید استنلس استیل، نیکل نقش مهمی در صنایع دیگر نیز ایفا میکند. به عنوان مثال، نیکل در تولید باتریهای قابل شارژ استفاده میشود. باتریهای لیتیوم – یونی، که در دستگاههای الکترونیکی قابل حمل مانند تلفن همراه و لپتاپ استفاده میشوند، نیز دارای کاتد حاوی نیکل هستند. همچنین، نیکل در صنعت فلزات پایه و آلیاژهای مختلف استفاده میشود و در تولید سکهها، جواهرات، و محصولات دیگر نقش دارد.
جدول مشخصات عنصر نیکل:
| عدد اتمی | 28 |
| نماد شیمیایی | Ni |
| وزن اتمی (جرم مولی) | 58.69 |
| نقطه ذوب (درجه سانتیگراد) | 1,453 |
| نقطه جوش (درجه سانتیگراد) | 2,732 |
| تراکم | 8.902 |
تاریخچه نیکل
این فلز از زمانهای باستانی بهطور طبیعی در برخی مناطق شناخته شده بود، اما بهطور رسمی توسط دانشمندان و شیمیدانان در قرن 18 میلادی شناسایی و شناخته شد. در سال 1751 میلادی، شیمیدان سوئدی آکسل فردیناند، کرومات نیکل (Nickel chromate) را بهعنوان یک عنصر جدید شناسایی کرد. واچمان، یک شیمیدان دیگر، نام “نیکل” را برای این عنصر انتخاب کرد و نام آن را از واژه آلمانی “Kupfernickel” که به معنی “شیطان مس” است، گرفت. این نام به دلیل وجود مادههای غیرمسی و معدنی که در معادن مس معمولاً با مس مخلوط بود، انتخاب شد.
نیکل در ابتدا بهطور عمده در صنعت استخراج مس مورد استفاده قرار میگرفت. با پیشرفت تکنولوژی و شناخت بیشتر دربارهٔ خواص نیکل، استفاده از آن در سایر صنایع نیز افزایش یافت. در قرن 19 میلادی، تولید نیکل با روشهایی مانند استخراج از کانیهای نیکل سولفیدی و تولید بهصورت الکترولیتی گسترش یافت.
امروزه، نیکل یکی از مواد استراتژیک و حیاتی در صنایع مختلف مانند خودروسازی، صنایع الکترونیکی، صنعت هوا و فضا، انرژی تجدیدپذیر، و صنایع شیمیایی است. تکنولوژیهای جدید و نیاز به فناوریهای پاک و پایدار، همچنین افزایش تولید خودروهای الکتریکی، به افزایش تقاضا برای نیکل در سالهای اخیر کمک کرده است.
نیکل در کجا یافت می شود؟
نیکل یک فلز انتقالی است و در طبیعت به صورت محدود یافت میشود. اما نیکل به صورت جایگزین قابل توجه برای بسیاری از فلزهای استراتژیک مانند مس، آهن، کبالت و غیره در معدنها و سنگهای معدنی وجود دارد. این عنصر از طریق فرآیندهای طبیعی مانند تشکیل سنگهای معدنی، تودههای مگمایی، تراکمهای سولفیدی و نیز از طریق فعالیتهای زمینشناسی و آتشفشانی به زمین منتشر میشود.
مهمترین منابع استخراج نیکل عبارتند از:
1. سولفیدهای نیکل: نیکل به صورت سولفیدها مانند پنتلندیت، پیرولوزیت و پیرتیت در معادن موجود است. برخی از معدنهای معروف شامل معدن نیکل Sudbury در کانادا و معدن نیکل Norilsk در روسیه است.
2. اکسیدهای نیکل: نیکل به صورت اکسیدهایی مانند نیکلیت و بریکسیت نیز در برخی از معادن یافت میشود.
3. کبالت نیکل: برخی از معادن کبالت، از جمله معدن کبالت نیکل، حاوی مقادیر قابل توجهی از نیکل هستند.
استخراج نیکل به وسیلهی معادنکاری صنعتی و فناوریهای مرتبط صورت میگیرد. در صنعت، نیکل استخراج شده به منظور استفاده در صنایع مختلف مانند فولادسازی، صنایع الکترونیک، صنعت خودروسازی، صنعت شیمیایی و غیره استفاده میشود.
کاربردهای نیکل
نیکل به عنوان یک فلز با خواص خاص در صنایع و وسایل مختلف استفاده میشود. مهمترین کاربردهای نیکل عبارتند از:
- نقش نیکل در انقلاب وسایل نقلیه الکتریکی: با افزایش حرکت جهانی به سمت حمل و نقل پایدار، وسایل نقلیه الکتریکی (EVs) شتاب بیشتری به دست آوردهاند. نیکل نقش مهمی در تولید باتریهای EV به ویژه در مواد کاتدی ایفا میکند. این بخش به اهمیت نیکل در فناوری EV پرداخته و در مورد چالشها و پیشرفتهای شیمی باتری و همچنین تأثیر آن بر بازار نیکل بحث میکند.
- تأثیر نیکل بر تولید فولاد ضد زنگ: فولاد ضد زنگ، فلزی است که به طور گسترده در ساخت و ساز، زیرساختها و بخشهای تولیدی مورد استفاده قرار میگیرد. این فلز به شدت به نیکل متکی است.
- کمک نیکل به سیستمهای انرژی تجدیدپذیر: منابع انرژی تجدیدپذیر مانند انرژی باد و خورشیدی به سیستمهای ذخیره انرژی کارآمد نیاز دارند. نیکل نقش مهمی در فناوریهای مختلف ذخیرهسازی انرژی، از جمله باتریهای نیکل-هیدروژن و باتریهای نیکل-آهن دارد.
- فلزات آلیاژی: نیکل به عنوان عنصر اصلی در تولید آلیاژهای مهمی مانند فولاد ضد زنگ (استیل) که شامل نیکل و کروم است، استفاده میشود. آلیاژهای نیکل-مس نیز در تولید کابلهای برق، پایپینگها و قطعات صنعتی استفاده میشوند.
- جواهرات: به دلیل ظاهر زیبا و ارزش بالای نیکل، این فلز در ساخت جواهرات مانند انگشترها، دستبندها، گردنبندها و گوشوارهها استفاده میشود. در این موارد، نیکل ممکن است به عنوان یک پوشش ضد حساسیت روی جواهرات مفید باشد.
- صنایع خودروسازی: در صنعت خودروسازی، نیکل در تولید قطعات مختلف مانند رینگها، سیم کویلها، ترمینالها و سیستم خنککننده خودرو استفاده میشود.
- صنایع شیمیایی: نیکل در تولید مواد شیمیایی مانند کودها، رنگها، پیگمنتها، کاتالیزورها و مواد حفاظتی به کار میرود.
- صنایع غذایی: در برخی فرآوردههای غذایی مانند تندیسهای شکلاتی، پوششهای آلومینیومی بر روی ظروف غذاخوری و همچنین در تولید تعدادی از افزودنیها و ویتامینها نیز از نیکل استفاده میشود.
این فقط برخی از مثالهای کاربرد نیکل در صنایع و وسایل مختلف است و استفادههای دیگر نیز وجود دارد.
کاربرد نیکل در الکترولیز و تولید هیدروژن
در الکترولیز، جریان الکتریکی از آب عبور داده می شود و هیدروژن و اکسیژن تولید می شود. الکترودهای فلزی در آب قرار می گیرند و جریان الکتریکی از طریق آنها عبور می کند. این باعث می شود که هیدروژن در کاتد (الکترود منفی) و اکسیژن در آند (الکترود مثبت) تولید شود.
از نیکل در الکترولیز استفاده می شود زیرا نیکل یک فلز واکنش پذیر است و این بدان معناست که می تواند به راحتی با اکسیژن آب واکنش دهد و هیدروژن آزاد کند. نیکل همچنین یک فلز با رسانایی الکتریکی بالا است که این بدان معناست که می تواند جریان الکتریکی را به خوبی هدایت کند. در نهایت نیکل یک فلز مقاوم در برابر خوردگی است که یعنی می تواند در برابر آب و سایر مواد شیمیایی پایدار باشد.
مطلب مرتبط: بهترین فلز برای تولید هیدروژن
نیکل به دلیل واکنش پذیری بالا، رسانایی الکتریکی بالا و مقاومت در برابر خوردگی، یک الکترود ایده آل برای الکترولیز است. این فلز می تواند به راحتی با اکسیژن آب واکنش دهد و هیدروژن آزاد کند. همچنین می تواند جریان الکتریکی را به خوبی هدایت کند که برای الکترولیز ضروری است. علاوه بر این، نیکل در برابر آب و سایر مواد شیمیایی پایدار است که باعث می شود برای الکترولیز در طیف گسترده ای از شرایط محیطی مناسب باشد.
البته، نیکل یک فلز گران قیمت نیست. بنابراین، از آن اغلب برای تولید هیدروژن در مقیاس بزرگ استفاده می شود. برای تولید هیدروژن در مقیاس کوچک، از فلزات ارزان تر مانند آلومینیوم یا روی استفاده می شود.
قیمت نیکل
قیمت نیکل تحت تأثیر عوامل متعددی قرار میگیرد. در زیر، برخی از عوامل تأثیرگذار بر قیمت نیکل را بررسی میکنیم:
- عرضه و تقاضا: عرضه و تقاضای نیکل در بازار، تأثیر مستقیمی بر قیمت آن دارد. اگر عرضه نیکل کاهش یابد و تقاضا برای آن افزایش یابد، قیمت نیکل معمولاً افزایش مییابد و بالعکس. عواملی مانند رشد صنایع استفاده کننده از نیکل (مانند صنایع فولاد، خودروسازی، الکترونیک و شیمیایی)، تغییرات در تقاضای جهانی و تحولات اقتصادی در کشورها میتوانند عوامل تعیین کننده در عرضه و تقاضا باشند.
- ذخایر معدنی: وجود و میزان ذخایر معدنی نیکل در جهان نیز تأثیرگذار بر قیمت آن است. هر چه ذخایر معدنی کمتر یا دسترسی به آنها محدودتر باشد، قیمت نیکل معمولاً افزایش مییابد.
- تولیدکنندگان و صادرکنندگان: تعداد و عملکرد تولیدکنندگان نیکل و صادرکنندگان این فلز نیز بر قیمت آن تأثیرگذار است. تغییرات در توان تولید کشورهای عمدهای مانند اندونزی، روسیه، کانادا و استرالیا، که جزء بزرگترین تولیدکنندگان نیکل هستند، میتواند قیمت را تحت تأثیر قرار دهد.
- تغییرات تجاری و سیاستهای تجاری: سیاستهای تجاری مانند تعرفهها، محدودیتها در صادرات و واردات، توافقنامههای تجاری و تحریمها نیز میتوانند بر قیمت نیکل تأثیرگذار باشند. تغییر در سیاستهای تجاری میتواند تعدادی از تولیدکنندگان را محدود کرده یا رقابت را کاهش دهد، که در نتیجه ممکن است قیمت نیکل را تحت تأثیر قرار دهد.
- نرخ تبدیل ارز: با توجه به اینکه بازار نیکل بینالمللی است، نرخ تبدیل ارز نیز نقشی مهم در تعیین قیمت نیکل ایفا میکند. تغییرات در نرخ ارز میتواند تأثیر مستقیم یا غیرمستقیمی بر قیمت نیکل داشته باشد.
لازم به ذکر است که بازار نیکل بسیار پویا است و تأثیرگذاری عوامل مذکور ممکن است در بازههای زمانی مختلف متفاوت باشد. همچنین، تحلیل دقیق و بروزترین اطلاعات در زمینه نیکل برای درک بهتر از روند قیمت آن توصیه میشود.
نیکل ژاپنی و قیمت آن
نیکل ژاپنی یا به زبان انگلیسی Japanese Nickel به یک نوع آلیاژ نیکل اطلاق میشود که دارای خواص خاصی است. این آلیاژ معمولاً شامل نیکل با مقدار بالا و عناصر دیگری مانند مس، روی و کبالت است. نیکل ژاپنی به دلیل ویژگیهای فیزیکی و شیمیایی خاص، در برخی صنایع و کاربردهای خاص مورد استفاده قرار میگیرد. برخی از ویژگیهای این آلیاژ عبارتند از:
1. مقاومت در برابر خوردگی: نیکل ژاپنی به دلیل حضور نیکل در آن، مقاومت بسیار بالایی در برابر خوردگی و اکسیداسیون دارد. این ویژگی آن را در برابر اثرات محیطی مانند رطوبت، اسیدها و بازها مقاوم میسازد.
2. مقاومت در برابر حرارت: نیکل ژاپنی قابلیت تحمل در دماهای بالا را دارد و مقاومت حرارتی بالایی دارد. این ویژگی آن را مناسب برای کاربردهایی مانند صنعت فولادسازی، پردازش حرارتی و ساخت قطعات در دماهای بالا میکند.
3. روشنایی و ظاهر زیبا: نیکل ژاپنی دارای ظاهری روشن و زیبا است که مناسب برای تزیینات، جواهرات و محصولات دیگر است.
4. مقاومت مکانیکی: این آلیاژ دارای مقاومت مکانیکی مناسبی است که آن را برای استفاده در قطعاتی با نیاز به مقاومت بالا مناسب میسازد.
از نیکل ژاپنی در صنایع مختلفی از جمله صنایع خودروسازی، هوافضا، الکترونیک، صنایع شیمیایی و صنعت فولادسازی استفاده میشود.
معادن نیکل در جهان
ذخایر نیکل در سراسر جهان وجود دارند و بسیاری از کشورها دارای ذخایر قابل توجهی هستند. در زیر، برخی از کشورهای دارای معادن نیکل بزرگ را ذکر میکنیم:
- اندونزی: اندونزی جزء بزرگترین تولیدکنندگان نیکل در جهان است. استخراج نیکل در این کشور از طریق معادنی مانند معدن سورینگ در جاوا و معدن پتیکا در سولاوسی صورت میگیرد.
- روسیه: روسیه یکی از بزرگترین تولیدکنندگان نیکل در جهان است. مناطقی مانند شبارتسک در سیبری و نیکل در منطقه مورمانسک شامل معادن نیکل مهم در روسیه هستند.
- کانادا: کانادا همچنین یکی از تولیدکنندگان بزرگ نیکل در جهان است. استان نیوفاندلند و لابرادور در شرق کانادا و منطقه سودبری در استان منیتوبا از جمله مناطقی هستند که معادن نیکل مهمی دارند.
- استرالیا: استرالیا نیز منابع قابل توجهی از نیکل دارد. استان وسترن استرالیا با مناطقی مانند کالدیکوتا و لیندرا در آن شامل معادن نیکل مهم در این کشور است.
- فیلیپین: فیلیپین همچنین یکی از تولیدکنندگان نیکل در جهان است. جزایر سولو و میندانائو در فیلیپین شامل معادن نیکل مهمی هستند.
علاوه بر این، برخی از دیگر کشورهایی که دارای معادن نیکل هستند عبارتند از: برزیل، کوبا، کلمبیا، نیو کالدونیا (منطقه وابسته به فرانسه)، جمهوری دموکراتیک کنگو و ایران.
تولید نیکل در ایران
ایران یکی از کشورهایی است که منابع غنی از سنگهای معدنی نیکل را در اختیار دارد. در حال حاضر، تولید نیکل در ایران از طریق معادنی مانند معدن چاهدار در استان آذربایجان شرقی و معدن کاموا در استان هرمزگان صورت میگیرد.
معدن چاهدار در آذربایجان شرقی یکی از بزرگترین معادن نیکل در جهان است. در این معدن، فرآیند استخراج و فرآوری نیکل انجام میشود. همچنین، معدن کاموه در هرمزگان نیز یکی دیگر از منابع نیکل در ایران است. همچنین، برنامههایی برای توسعه صنعت نیکل در ایران وجود دارد. با بهرهبرداری از ظرفیتهای معدنی و پتانسیلهای بالقوه دیگر، قابلیت توسعه تولید نیکل در ایران وجود دارد.
تولید نیکل در ایران تحت نظارت و کنترل وزارت صنعت، معدن و تجارت و سازمان زمینشناسی و اکتشافات معدنی کشور انجام میشود.
جمعبندی
تقاضای نیکل به دلیل نقش حیاتی آن در وسایل نقلیه الکتریکی، تولید فولاد ضد زنگ، سیستم های انرژی تجدیدپذیر و کاربردهای مختلف صنعتی، به طور پیوسته در صنایع مختلف به رشد خود ادامه می دهد. درک کاربردهای چند وجهی و پویایی بازار پیرامون نیکل برای سرمایه گذاران، متخصصان صنعت و سیاست گذاران ضروری است تا چشم انداز در حال تحول را درک کنند و از فرصت های بالقوه ارائه شده توسط این فلز همه کاره استفاده کنند.
پرسش و پاسخ
از ترکیب نیکل کروم و آهن چه چیزی حاصل میشود؟
ترکیب نیکل، کروم و آهن به عنوان آلیاژ آهن نیکل کروم (Iron-Nickel-Chromium Alloy) شناخته میشود. این آلیاژ معمولاً شامل مقادیر متفاوتی از نیکل، کروم و آهن است و به دلیل خواص ویژهای که دارد، در صنایع مختلف به عنوان مواد ساختاری و مقاوم در برابر خوردگی استفاده میشود. با ترکیب این سه عنصر، آلیاژهای آهن نیکل کروم به خواصی مانند مقاومت بالا در برابر خوردگی، مقاومت در برابر حرارت و استحکام مکانیکی مناسب دست مییابند. آلیاژهای مختلف آهن نیکل کروم ممکن است در ترکیبات مختلفی از این عناصر تولید شوند، مانند آلیاژهای زیر:
- آلیاژ اینکونل Inconel (Ni-Cr-Fe)
- آلیاژ هستلوی Hastelloy (Ni-Cr-Fe)
- آلیاژ اینوار Invar (Fe-Ni)
- فولاد ضد زنگ Stainless Steel (Fe-Cr-Ni)
از آلیاژ آهن نیکل کروم در صنایع خودروسازی، هوافضا، صنایع شیمیایی، نفت و گاز، صنایع الکترونیکی و ساخت و ساز استفاده میشود. به عنوان مثال، استفاده از استیل ضد زنگ (Stainless Steel) که یک نوع آلیاژ آهن نیکل کروم است، در ساخت قطعات خودروها، وسایل آشپزخانه، تجهیزات پزشکی و سازههای ساختمانی بسیار رایج است.
آیا نیکل به آهن ربا می چسبد؟
خیر، نیکل مغناطیسی نیست و به آهنربا نمیچسبد. نیکل یک فلز غیر مغناطیسی در نظر گرفته میشود، به این معنی که خاصیت مغناطیسی ذاتی ندارد. با این حال، توجه به این نکته مهم است که نیکل در صورت ترکیب با سایر مواد مغناطیسی یا آلیاژها میتواند جذب آهنربا شود.
یون نیکل چند بار دارد؟
یون نیکل معمولاً دو حالت بار دار دارد، به شرح زیر:
1. یون نیکل دو باره (Ni²⁺): در این حالت، یون نیکل دو بار مثبت دارد. این حالت از رایجترین حالات یونی نیکل است و بیشتر در ترکیبات شیمیایی نیکل مشاهده میشود.
2. یون نیکل سه باره (Ni³⁺): در برخی ترکیبات شیمیایی و شرایط خاص، نیکل میتواند سه بار مثبت داشته باشد. این حالت کمتر رخ میدهد و در شرایط خاصی از تعادل اکسایش-ترکیب نیکل ممکن است به دست آید.
مقدار بار یونهای نیکل به عوامل مختلفی مانند شرایط شیمیایی و الکتروشیمیایی وابسته است.
نیکلوزاماید چیست؟
نیکلوزاماید (Nickelodeamide) که همچنین با نام آمید نیکل (Nickel amide) شناخته میشود. این ترکیب شیمیایی، یک ترکیب آلی است که شامل نیکل و گروه آمید (-CONH₂) است. نیکلوزاماید در واقع نمایندهای از ترکیبات آلی نیکل است که میتواند در ترکیبات شیمیایی مورد استفاده قرار گیرد. از نیکلوزاماید به عنوان کاتالیزور در واکنشهای شیمیایی استفاده میشود، به خصوص در واکنشهایی که نیاز به فعالسازی نیکل دارند.
همچنین، نیکلوزاماید ممکن است در ترکیبات دارویی، پیگمنتها، رنگها، و مواد افزودنی دیگر مورد استفاده قرار گیرد. با این حال، به دلیل حساسیت برخی افراد نسبت به نیکل، استفاده از نیکلوزاماید در برخی محصولات و کاربردها ممکن است محدود شود و نیاز به احتیاط داشته باشد.
نیکل شهاب سنگ چیست؟
اصطلاح “نیکل شهاب سنگ” (Nickel-iron meteorite) به نوعی به شهاب سنگی اطلاق میشود که دارای ترکیبات نیکل و آهن است. این شهاب سنگها به عنوان یکی از انواع شهاب سنگها معروف هستند و معمولاً در ارتباط با سیستم خورشیدی ما در مناطق دورترین بخشهای آن و مخصوصاً در نزدیکی بدنههای سیارهای مانند سیاره زمین قرار دارند.
نیکل شهاب سنگها اغلب دارای ترکیباتی هستند که شامل 10% تا 30% نیکل و مابقی آهن میباشد. این ترکیب آلیاژی از نیکل و آهن باعث میشود که نیکل شهاب سنگها دارای خواص خاصی مانند مقاومت مکانیکی بالا و مغناطیسی بودن باشند. همچنین، نیکل شهاب سنگها ممکن است دارای ساختارهای خاصی مانند خطوط و رگههای ویژه در سطح خود باشند. از آنجا که نیکل شهاب سنگها دارای نیکل هستند، این شهاب سنگها معمولاً اهمیت اقتصادی دارند و ممکن است به عنوان منابع نیکل در صنایع مورد استفاده قرار بگیرند.
نیکل سیلور چیست؟
نیکل سیلور (Nickel Silver) در واقع یک آلیاژ است و نامی است که برای ترکیبات آلیاژی استفاده میشود که شامل نیکل، مس و روی است. این آلیاژ حاوی نقره نیست، اما به دلیل شباهت رنگی و برخی ویژگیها، به آن نام “نیکل سیلور” داده شده است.
نیکل سیلور به دلیل خواصی مانند مقاومت در برابر خوردگی، مقاومت مکانیکی و ظاهری شبیه به نقره، در صنایع مختلف استفاده میشود. برخی از کاربردهای رایج نیکل سیلور شامل ساخت قطعات ساعت، جواهرات، سازههای موسیقی (مانند سازهای بادی و زهی)، تجهیزات الکترونیکی و لوازم استفاده روزمره مانند قاشق و چنگال، لیوان و ظروف غذاخوری است.
سولفات نیکل چیست؟
سولفات نیکل (Nickel sulfate) یک ترکیب شیمیایی است که شامل نیکل و یون سولفات (SO₄²⁻) است. فرمول شیمیایی آن NiSO₄ است. نیکل سولفات اغلب به صورت ضربهپذیر بلورهای سفید یا سبز رنگ یافت میشود و در آب قابل حل است. این ترکیب در بسیاری از صنایع و کاربردها مورد استفاده قرار میگیرد، به عنوان مثال:
1. الکتروپلیتینگ (Electroplating): نیکل سولفات برای روکش کردن قطعات فلزی با لایه نیکل به منظور افزایش مقاومت در برابر خوردگی، تغییر رنگ و ظاهر، افزایش سختی و غیره در صنایع مانند خودروسازی، جواهرسازی و الکترونیک استفاده میشود.
2. تولید باتریها: نیکل سولفات در صنایع باتریسازی، به خصوص در باتریهای قلیایی، استفاده میشود.
3. صنایع رنگسازی: نیکل سولفات در تولید رنگها، پیگمنتها و رنگدانهها استفاده میشود.
4. صنایع کاغذسازی: این ترکیب برای بهبود استحکام کاغذ استفاده میشود.
5. صنایع کشاورزی: نیکل سولفات به عنوان منبعی از نیکل در محصولات کشاورزی مورد استفاده قرار میگیرد.
در همه موارد استفاده از نیکل سولفات، نیاز است که اصول ایمنی و آشنایی کامل با راهنماها و دستورالعملهای ایمنی مربوطه را رعایت کنید.
نیکل چند ظرفیتی است؟
نیکل، به عنوان یک عنصر شیمیایی، بر اساس مقدار الکترونهای خارجی خود، چند ظرفیتی است. ظرفیت نیکل برابر است با 28. این به این معنی است که نیکل در لایه الکترونی خارجی خود میتواند حداکثر 28 الکترون داشته باشد. نیکل، در ترکیبات شیمیایی خود و آلیاژها، میتواند به صورت مختلفی الکترونها را اختصاص دهد و نقشهای مختلفی را در واکنشها و واکنشهای الکتروشیمیایی ایفا کند. مثلاً در برخی ترکیبات، نیکل میتواند به عنوان یک نوسانگر الکترونی با عنوان نیکل (II) عمل کند که دو الکترون برای انتقال در اختیار دارد. همچنین، نیکل به عنوان نیکل (0) نیز میتواند به عنوان یک کاتالیزور الکترونیک در برخی واکنشها عمل کند. به طور کلی، ظرفیت الکترونیکی نیکل و توزیع الکترونی آن در لایههای الکترونی مختلف، نقش مهمی در خواص و واکنشهای شیمیایی آن دارد.
نیکل چگونه وارد خاک میشود؟
نیکل میتواند به صورت طبیعی وارد خاک شود و یا از طریق فعالیتهای انسانی به خاک اضافه شود. روشهای اصلی ورود نیکل به خاک عبارتند از:
1. فرآیندهای طبیعی: نیکل در برخی مناطق به صورت طبیعی در سنگها و سنگهای معدنی وجود دارد. از طریق فرآیندهای زمینشناسی مانند آتشفشانی، ارتباط آب و سنگ، فرآیندهای آبی و هواشناسی و غیره، نیکل از سنگها جدا شده و وارد خاک میشود.
2. فعالیتهای انسانی: نیکل میتواند از طریق فعالیتهای انسانی وارد خاک شود، از جمله، استخراج معادن و کاربردهای صنعتی که در طی آن استفاده از نیکل در صنایع مختلف مانند خودروسازی، الکترونیک، صنایع شیمیایی و غیره، ممکن است منجر به آلودگی خاک شود. این میتواند به صورت غیرمنظم از طریق پسماندها، انتشارات هوا، آبهای بازیافت شده و غیره رخ دهد.
علاوه بر این، نیکل نیز ممکن است به صورت خاص در مناطقی که فعالیتهای صنعتی یا معدنی مرتبط با نیکل انجام میشود، به خاک اضافه شود. این مسائل میتواند باعث ایجاد آلودگی خاک به نیکل شود، که در برخی موارد میتواند منجر به مشکلات زیستی محیط و بهداشتی شود.
کدام سکه ها نیکل دارند؟
چندین سکه در جهان حاوی نیکل هستند. به عنوان مثال:
1. سکه دلار کانادا: سکه دلار کانادا (Canadian dollar)، یک سکه فلزی است که شامل نیکل است. در حقیقت، این سکه به طور رایج به عنوان “لونی” (Loonie) شناخته میشود.
2. سکه دلار استرالیا: سکه دلار استرالیا (Australian dollar) نیز شامل نیکل است. این سکه در بازار عمومی با نام “دالاری” (Dollar coin) شناخته میشود.
3. سکه یورو: برخی از سکههای یورو نیز حاوی نیکل هستند. سکههای 1 و 2 یورویی از آلیاژی تشکیل شدهاند که شامل نیکل است.
آیا نیکل سرطان زا است؟
مطالعات صورت گرفته تاکنون نشان دادهاند که نیکل ممکن است در برخی شرایط و در موارد خاص، به عنوان یک عامل سرطان زا عمل کند. این ویژگی سرطان زا به نیکل در ارتباط با تماس مستقیم و طولانی مدت با آن و یا تماس با مقادیر بالای آن در محیط کار مرتبط است. به عنوان مثال، کارکنانی که در صنایعی که از نیکل استفاده میکنند (مانند صنایع فلزی، صنایع شیمیایی و غیره) مشروط بر تماس مستقیم و مستمر با نیکل، ممکن است در برابر خطرات سرطان زای نیکل قرار داشته باشند.
مهم است بدانید که خطر سرطانزایی نیکل بستگی به غلظت، شکل و مسیر اعمال آن دارد. اگر نیکل به صورت خام و بدون پردازش به مقادیر بالایی از بدن وارد شود، میتواند خطرات سرطان زایی را افزایش دهد. اما در موارد استفاده عمومی از نیکل در محصولاتی مانند جواهرات، ساعتها، سکهها و غیره، خطر سرطان زایی نیکل بسیار کمتر است، زیرا معمولاً در مقادیر بسیار کمتری و در شکلهایی که به طور مستقیم با پوست وارد تماس نمیشوند، استفاده میشود.
منابع مهم در این زمینه شامل سازمان بهداشت جهانی (WHO)، سازمان حفاظت محیط زیست آمریکا (EPA) و سازمان حفاظت از محیط زیست اروپا (EEA) هستند.
آیا نیکل رساناست؟
بله، نیکل یک رسانا (کانداکتور) خوب برق است. این به معنای این است که نیکل توانایی انتقال جریان الکتریکی را دارد. به عنوان یک فلز، نیکل دارای خواص رسانایی بالایی است و میتواند جریان الکتریکی را به خوبی عبور دهد. بنابراین، نیکل در مصارف مختلفی از جمله الکترونیک، صنعت برق، تولید باتری، صنایع خودروسازی و غیره به عنوان رسانا استفاده میشود.
آیا نیکل زنگ میزند؟
نیکل به طور کلی زنگ نمیزند. اما با توجه به آلیاژهایی که شامل نیکل هستند، ممکن است خواص متفاوتی داشته باشند. در ضمن، در صورتی که نیکل آلایشهایی مانند روی یا اکسید بپذیرد، ممکن است زنگ خوردگی را در محصولاتی که شامل آن است، ایجاد کند. این امر ممکن است در صورت تماس نیکل با آب، هوا یا عوامل دیگری که میتوانند راکتیو باشند، رخ دهد. به هر حال، برای کاربردهایی که نیکل در آن استفاده میشود، معمولاً از روشهایی مانند روکش کردن یا آلیاژسازی استفاده میشود تا ضد زنگ و مقاوم در برابر خوردگی شود.
آیا نیکل سمی است؟
مقادیر زیاد نیکل در بدن ممکن است برای برخی افراد حساس، مانند افرادی که دارای حساسیت به نیکل هستند، مشکل ساز شود. این حساسیت میتواند علائمی مانند خارش، قرمزی و التهاب پوست، تورم و تحریک را به همراه داشته باشد. برای کاهش خطر احتمالی، در صورتی که به نیکل حساس هستید، میتوانید از جواهرات با پوشش ضد حساسیت، سکهها و ساعتها با بدنه غیرآلرژیک و محصولات مشابه استفاده کنید. همچنین، در صورت ایجاد علائم حساسیت پس از تماس با نیکل، بهتر است به پزشک مراجعه کنید تا تشخیص و درمان مناسب صورت پذیرد.
آیا تبدیل باتری نیکل به لیتیوم امکان دارد؟
متأسفانه، تبدیل یک باتری نیکل به یک باتری لیتیوم به صورت مستقیم امکانپذیر نیست. باتریهای نیکل و باتریهای لیتیوم از تکنولوژیهای متفاوتی استفاده میکنند و دارای ساختارهای مختلفی هستند. باتریهای نیکل، معمولاً در فرمتهایی مانند باتریهای نیکل-کادمیوم (NiCd) یا باتریهای نیکل-متال هیدرید (NiMH) وجود دارند. این باتریها از ترکیبات نیکل و فلزات دیگر مانند کادمیوم یا فلزات هیدروژن استفاده میکنند.
باتریهای لیتیوم، به عنوان مثال باتریهای لیتیوم-یون (Li-ion)، از فناوری متفاوتی استفاده میکنند و در طیف وسیعی از دستگاههای الکترونیکی استفاده میشوند. باتریهای لیتیومی بر پایه ترکیبات شیمیایی لیتیم و کاتد متنوعی مانند اکسید لیتیم، کوبالت، منگنز و نیکل ساخته میشوند.
تشخیص نیکل از نقره چگونه است؟
برای تشخیص نیکل از نقره، میتوانید از روشهای زیر استفاده کنید:
1. آزمایش شیمیایی با آزمون نیکل: یک آزمون شیمیایی معمول برای تشخیص نیکل، آزمون دیمتیل گلوکسیم است. شما میتوانید نمونهای از فلز یا ترکیب حاوی نیکل را با دیمتیل گلوکسیم مخلوط کنید. اگر تشکیل رنگ صورت گرفته و یک محلول صورت گرفت، این نشانه از وجود نیکل است. با این روش، نقره و نیکل تفاوت قابل تشخیصی در تشکیل رنگ ایجاد میکنند.
2. آزمایش الکتروشیمیایی: از روش الکتروشیمیایی نیز میتوان برای تشخیص نیکل استفاده کرد. برای انجام این آزمایش، شما نیاز به یک سلول الکتروشیمیایی دارید که شامل دو الکترود (کاتد و آند) و یک محلول الکترولیتی است. با قرار دادن نمونه در محلول الکترولیتی و اعمال پتانسیل الکتریکی، اگر جریان الکتریکی از دستگاه عبور کند، نشان از وجود نیکل است. در صورت وجود نقره، جریان الکتریکی ایجاد نخواهد شد.
3. آزمایش آتومیزاسیون: آزمایش آتومیزاسیون یک روش دقیق برای تشخیص نیکل است. در این آزمایش، از روش همراه با آتومیزاسیون، نمونه مورد بررسی را تحت تأثیر یک پلاسما قرار میدهند. با تحلیل نقره به وسیله آتومیزاسیون، نشانههای نیکل در طیف جذب ایجاد میشود. با مقایسه طیف جذب نمونه با طیف جذب استاندارد نیکل، میتوان نیکل را تشخیص داد.
این روشها تنها برخی از روشهای ممکن برای تشخیص نیکل از نقره هستند. در صورتی که نمیتوانید خود این آزمایشها را انجام دهید، میتوانید به آزمایشگاههای تخصصی یا به کمک متخصصان مربوطه مراجعه کنید تا بتوانند نمونه شما را تجزیه و تحلیل کنند و نیکل و نقره را از یکدیگر تشخیص دهند.
جداسازی نیکل از سکه چگونه انجام می شود؟
جداسازی نیکل از سکه یا هر شیء دیگری که حاوی نیکل باشد، ممکن است نیازمند مراحل و فرآیندهای مختلف باشد. این فرآیندها به ویژگیهای متفاوت مواد و شرایط خاص بستگی دارد. در ادامه، روشی کلی برای جداسازی نیکل از سکه را توضیح میدهیم:
1. شناسایی نوع سکه: قبل از هر چیز، باید مطمئن شوید که سکه واقعاً حاوی نیکل است. برخی سکهها از جنس آلیاژهای دیگری مانند مس یا برنج هستند. بنابراین، ابتدا باید مطمئن شوید که سکه حاوی نیکل است.
2. استفاده از مواد شیمیایی: یکی از روشهای متداول برای جداسازی نیکل از سکه استفاده از مواد شیمیایی است. برای مثال، میتوانید از اسیدهای قوی مانند اسید نیتریک یا اسید کلریدریک استفاده کنید. این اسیدها ممکن است توانایی داشته باشند تا آلیاژهای دیگر را حل کرده و نیکل را جدا کنند.
3. استفاده از فرآیندهای الکتروشیمیایی: فرآیندهای الکتروشیمیایی نیز میتوانند برای جداسازی نیکل از سکه مورد استفاده قرار بگیرند. این شامل استفاده از الکترولیز و استخراج الکترولیتی میشود. در این روش، سکه به عنوان کاتد در الکترولیز استفاده میشود و نیکل از سطح سکه جدا میشود.
4. استفاده از فرآیندهای حرارتی: فرآیندهای حرارتی نیز میتوانند در جداسازی نیکل مفید باشند. مثلاً میتوانید سکه را با استفاده از حرارت بسیار بالا بیدرنگ یا در یک فرآیند گرمایش و سرد شدن تکراری تحت تأثیر قرار دهید تا اجزای آلیاژ تباشر کنند و نیکل جدا شود.
مهم است که بدانید، جداسازی نیکل از سکه یا هر مادهای دیگری ممکن است نیازمند مهارت، تجهیزات خاص و شرایط ایمنی خاص باشند. بهتر است این کار را توسط متخصصان مجرب یا در آزمایشگاههای تخصصی انجام دهید. همچنین، در نظر داشته باشید که در برخی مناطق قوانین مربوط به تجارت و معدن ممکن است محدودیتها و مقرراتی داشته باشد.
جداسازی نیکل از مس چگونه انجام می شود؟
برای جداسازی نیکل از مس، میتوانید از روشهای مختلفی استفاده کنید. در زیر چند روش کلی برای جداسازی نیکل از مس توضیح داده شده است:
1. روش انتقال فاز: در این روش، میتوانید از تفاوت در حلالیت نیکل و مس در یک حلال استفاده کنید. یکی از روشهای معروف انتقال فاز، استفاده از حلالیت نیکل در اسید سولفوریک است. شما میتوانید مخلوط مس و نیکل را در اسید سولفوریک حل کنید تا نیکل حل شده و مس به صورت جامد رسوب شود. سپس میتوانید نیکل را از محلول استخراج کرده و جدا کنید.
2. روش الکترواستخراج: در این روش، از اختلاف در پتانسیل الکتریکی نیکل و مس استفاده میشود. با استفاده از سلول الکترواستخراج، مس و نیکل را به عنوان الکترودها در نظر بگیرید. با اعمال پتانسیل الکتریکی، نیکل به عنوان کاتد در الکترود نیکل رسوب میشود و مس به عنوان آند در الکترود مس ذوب میشود. سپس میتوان نیکل را از الکترود جدا کرده و به دست آورد.
3. روش استخراج با استفاده از حلالهای گوگردی: حلالهای گوگردی میتوانند برای جداسازی نیکل از مس مفید باشند. در این روش، میتوانید از تفاوت حلالیت نیکل و مس در حلالهای گوگردی استفاده کنید. با افزودن یک حلال گوگردی مناسب به مخلوط مس و نیکل، مس به صورت جامد رسوب میکند و نیکل در محلول حل میشود. سپس میتوانید نیکل را از محلول استخراج کرده و جدا کنید.
حذف نیکل از پساب چگونه انجام میشود؟
حذف نیکل از پساب یک فرآیند مهم است که در صنایع و واحدهای تولیدی که با نیکل سر و کار دارند، انجام میشود. در زیر روشهای متداول برای حذف نیکل از پساب را شرح میدهیم:
1. فرآیند ترسیب شیمیایی: این روش شامل استفاده از مواد شیمیایی خاص است که با نیکل واکنش میدهند و نیکل را به صورت رسوبی جدا میکنند. برای مثال، اکسیدهای فلزاتی مانند هیدروکسید سدیم یا کربنات سدیم میتوانند استفاده شوند. این مواد به پساب اضافه شده و با نیکل واکنش داده میشوند تا نیکل به صورت رسوبی جدا شود. سپس رسوبات نیکل میتوانند با روشهای جداسازی مکانیکی مانند روش سنتریفوژ جدا شوند.
2. فرآیند جذب: در این روش، جاذبهای شیمیایی و طبیعی خاص مورد استفاده قرار میگیرند.
حساسیت با نیکل و راه درمان آن چیست؟
درمان حساسیت نیکل شامل تسکین علائم و پیشگیری از تماس با نیکل است. در ادامه، تعدادی اقدامات درمانی و پیشگیری را برای حساسیت نیکل ذکر میکنیم:
1. استفاده از کرمها یا محصولات ضد التهاب: برای تسکین علائم حساسیت نیکل، میتوانید از کرمها یا محصولات ضد التهاب استفاده کنید. این محصولات میتوانند تحریک و التهاب را کاهش داده و علائم را تسکین دهند.
2. استفاده از آنتیهیستامینها: در صورت بروز علائم آلرژی مانند خارش و التهاب پوست، ممکن است پزشک آنتیهیستامینها را تجویز کند. این داروها به کنترل علائم آلرژی و تسکین خارش کمک میکنند.
3. اجتناب از تماس با نیکل: برای پیشگیری از تماس با نیکل و ایجاد حساسیت، میتوانید اقدامات زیر را انجام دهید:
– استفاده از جواهرات ضد حساسیت: جواهرات با روکش ضد حساسیت یا ساخته شده از موادی مانند استیل ضد زنگ، طلا یا نقره با عیار بالا ممکن است کمک کند.
– استفاده از لباسهای ضد حساسیت: در صورتی که بر روی پوست با حساسیت نیکل تماس برقرار میکنید، از لباسهای ضد حساسیت استفاده کنید.
– اجتناب از موادی که حاوی نیکل هستند: مواد مانند سکه، کلید، سوپاپهای فلزی و غیره که ممکن است حاوی نیکل باشند، باید از آنها دوری کنید.
4. مشاوره پزشک: در صورت بروز حساسیت نیکل و علائم شدید، بهتر است با پزشک خود مشورت کنید. پزشک میتواند تشخیص دقیق برای شما قرار داده و درمان مناسب را تجویز کند.
آبکاری نیکل چیست؟
آبکاری نیکل یک فرایند شیمیایی است که در آن لایههای نیکل بر روی یک سطح فلزی ایجاد میشود. این فرآیند به عنوان یک روش پوشش دهی مورد استفاده قرار میگیرد و در اکثر موارد برای بهبود ظاهر و مقاومت به خوردگی و سایر خواص فیزیکی فلزات استفاده میشود. فرآیند آبکاری نیکل عموماً شامل مراحل زیر است:
1. پیشآبکاری: این مرحله شامل تمیز کردن سطح فلزی است. اینکار با استفاده از مواد شیمیایی مانند محلولهای آلکالایی (مثل هیدروکسید سدیم) یا اسیدی (مثل اسید سولفوریک) انجام میشود تا ذرات گرد و غبار، روغن، آلودگیها و لایههای قبلی روی سطح فلزی حذف شوند.
2. آبکاری الکترولیتیک: در این مرحله، سطح فلزی به عنوان کاتد درون یک محلول الکترولیتی (معمولاً حاوی نیترات نیکل) قرار میگیرد. با اعمال جریان الکتریکی، یونهای نیکل موجود در الکترولیت به صورت برقشیمیایی به سطح فلزی واکنش میکنند و لایه نیکل به صورت الکترولیتی روی سطح فلزی تشکیل میشود. ضخامت و خواص این لایه میتواند با تنظیم شرایط الکترولیت و پارامترهای فرایند تغییر کند.
3. پسآبکاری: پس از آبکاری الکترولیتیک، سطح فلزی با آب شسته میشود تا اثرات الکترولیت روی سطح کاهش یابد و لایه نیکل پایدارتر شود. همچنین، ممکن است از موادی مانند پسآبکاریکنندهها یا محلولهای ضد زنگ استفاده شود تا خواص مورد نیاز به دست آید.
آبکاری نیکل میتواند در بسیاری از صنایع مورد استفاده قرار بگیرد، از جمله صنایع خودروسازی، الکترونیک، جواهرسازی و ساعت سازی، تجهیزات آشپزخانه و غیره.
حلال نیکل به محلولی گفته میشود که نیکل در آن به صورت یونی حل شده است. این حلالها معمولاً شامل مواد شیمیایی و محلولهای الکترولیتی هستند که قادر به حل نیکل هستند و از آن به عنوان منبع نیکل برای فرآیندهای صنعتی و پژوهشی استفاده میشود.
یکی از حلالهای معروف برای حل نیکل، اسید نیتریک (HNO3) است. اسید نیتریک با قدرت اکسیدکنندگی خود میتواند نیکل را به صورت یونی (معمولاً نیکل(II)) حل کند. در این حالت، نیکل در محلول به صورت یونهای نیکل با بار مثبت و متعادل (Ni2+) و یونهای هیدروکسید (OH-) حضور دارد.
علاوه بر اسید نیتریک، سایر حلالها مانند اسید سولفوریک (H2SO4) و کلرید نیکل (NiCl2) نیز به عنوان حلالهای نیکل مورد استفاده قرار میگیرند. این حلالها بسته به نیازهای فرآیند مورد استفاده قرار میگیرند و میتوانند در فرآیندهای مختلف شیمیایی و صنعتی از جمله آبکاری، روشهای تصفیه و جداسازی نیکل و تهیه ترکیبات نیکلی مورد استفاده قرار بگیرند.
خواص نیکل برای بدن چیست؟
نیکل یک عنصر کمیاب است و در بدن انسان به صورت کمی وجود دارد. هرچند نیکل یک عنصر ضروری برای عملکرد بعضی از آنزیمها و فرآیندهای بیوشیمیایی است، اما مقدار مورد نیاز بسیار کم است و اکثر افراد نیاز به مکمل نیکل ندارند. در زیر برخی از خواص نیکل برای بدن ذکر شده است:
1. مشارکت در فعالیت آنزیمها: نیکل در ساختار برخی از آنزیمها حضور دارد و در فعالیت آنها نقش دارد. این آنزیمها به عنوان کاتالیزورها در واکنشهای بیوشیمیایی و فرآیندهای متابولیکی مختلف مهم هستند.
2. تأثیر بر فعالیت ایمنی: برخی از تحقیقات نشان میدهند که نیکل میتواند تأثیری بر روی سیستم ایمنی داشته باشد و برخی از فعالیتهای سلولهای ایمنی را تنظیم کند.
3. مشارکت در فرآیندهای بیولوژیکی: نیکل در برخی از فرآیندهای بیولوژیکی مانند متابولیسم کبد، تعادل اسید-باز بدن و جذب و استفاده از مواد مغذی نقش دارد.
فلزات, مقالات در گروه صبا | نویسنده : امید مرادی | بروزرسانی : 24 آذر 1402