عناصر مختلف جدول تناوبی هر کدام تاریخچهای غنی و پربار از کشف تا استفاده دارند. داستان هر کدام از این عناصر که بعضی از آنها فلز هستند و برخی دیگر نافلز، بسیار جالب و شنیدنی است. رازهای بسیاری در بعضی از این عناصر نهفته است که همچنان دانشمندان به دنبال کشف آنها هستند. یکی از این عناصر، مندلیفیم نام دارد که این عنصر به افتخار دیمیتری ایوانوویچ مندلیف، شیمیدان برجسته روسی و خالق جدول تناوبی، به این نام، نامگذاری شده است. در این مقاله به بررسی تاریخچه مندلیفیم، از کشف تا کاربردهای آن میپردازیم.
فهرست مطالب
مندلیفیم چیست؟
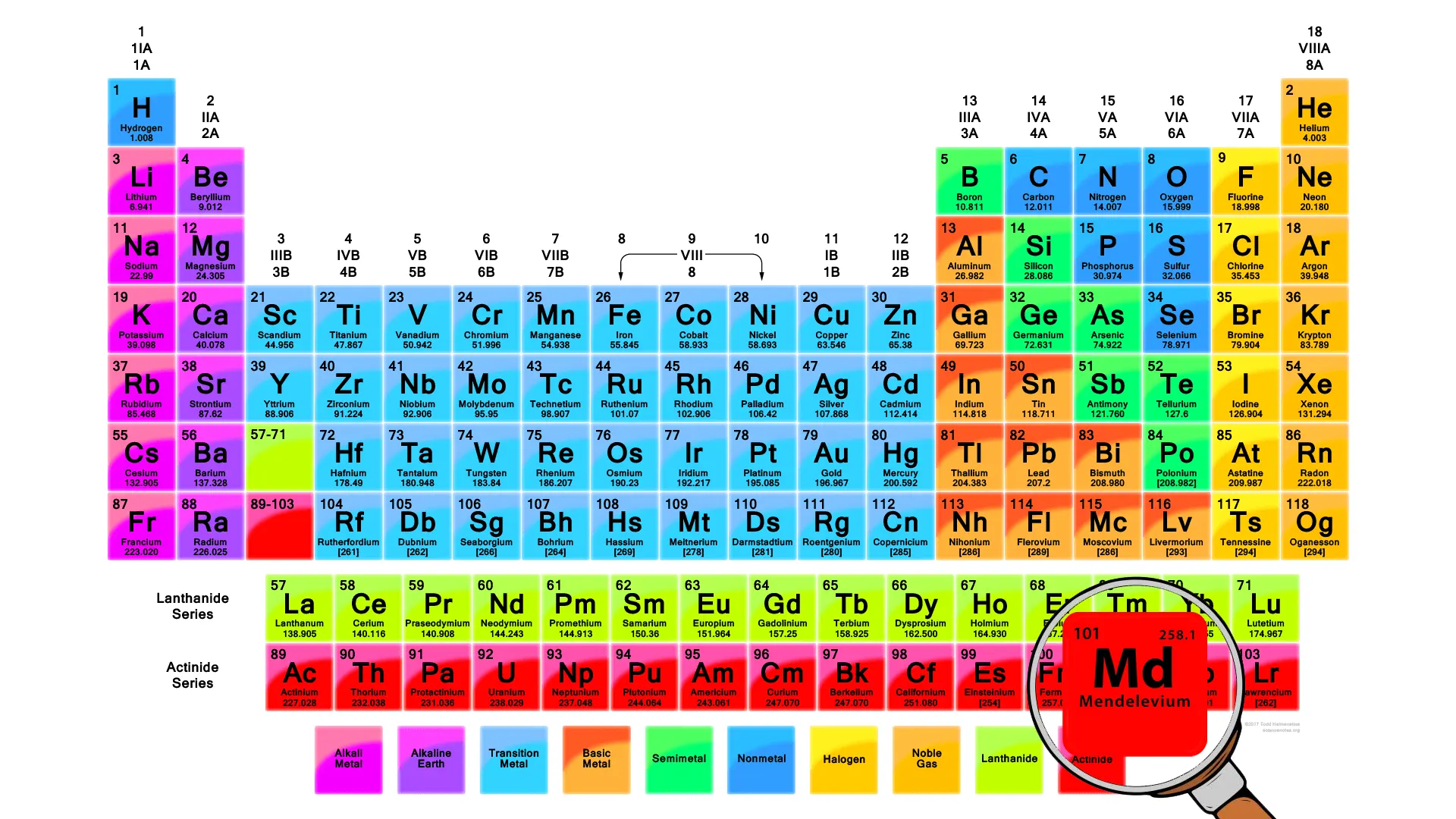
مندلیفیم (به انگلیسی Mendelevium) یک عنصر شیمیایی مصنوعی با نماد Md و عدد اتمی 101 است. این یک فلز رادیواکتیو ترانس اورانیوم در سری اکتینیدها است. مندلیفیم معمولاً با بمباران انیشتنیم با ذرات آلفا تولید می شود. این عنصر به افتخار دیمیتری ایوانوویچ مندلیف، شیمیدان برجسته روسی و خالق جدول تناوبی، نامگذاری شده است. مندلویوم فقط برای تحقیقات استفاده میشود و در حال حاضر کاربرد دیگری ندارد.
عنصر مندلیفیم در حقیقت صد و یکمین عنصر از جدول تناوبی عناصر بوده که در گروه IIIB و تناوب هفتم جدول تناوبی قرار گرفته است. عنصر مندلیفیم یک فلز واسطه (Transition Metals) رادیواکتیو، احتمالا به رنگ سفید، نقره ای و یا خاکستری (رنگ آن ناشناخته است) و از عناصر مصنوعی گروه اکتینیدها است.
این فلز با عناصر اسکاندیم (Sc)، ایتریم (Y) و لانتان (La)، در گروه سه واسطه جدول تناوبی عناصر قرار دارد. مندلیفیم در واقع عنصری است از نوع ترانزورانیک. عنصرهای ترانزورانیک، عنصرهایی با عدد اتمی بیشتر از 92 (عدد اتمی اورانیوم) هستند. این عنصرها به طور طبیعی در زمین یافت نمیشوند و به صورت مصنوعی در آزمایشگاهها تولید میشوند. اولین عنصر ترانزورانیک، نپتونیم، در سال 1940 توسط ادوین مک میلان و فیلیپ هابل در دانشگاه کالیفرنیا، برکلی سنتز شد. از آن زمان، حدود 20 عنصر ترانزورانیک دیگر سنتز شدهاند. عنصرهای ترانزورانیک ناپایدار هستند و به طور رادیواکتیو تجزیه میشوند. آنها همچنین فلزات سنگین هستند و معمولاً سمی هستند.
جدول مشخصات عنصر مندلیفیم
| عدد اتمی | 101 |
| نماد شیمیایی | Md |
| جرم اتمی | 258 |
| نقطه ذوب (درجه سانتیگراد) | 827 |
| نقطه جوش (درجه سانتیگراد) | 1027 |
| حالت | جامد در دمای اتاق |
| رنگ | نقره ای سفید |
ایزوتوپهای عنصر مندلیفیم
تاکنون 17 ایزوتوپ از مندلیفیم با عدد جرمی بین 245 تا 260 شناسایی شده است. پایدارترین ایزوتوپ مندلیفیم Md-258 با نیمه عمر 51.5 روز است. ایزوتوپهای مندلیفیم معمولاً با بمباران انیشتنیم-253 با ذرات آلفا یا با بمباران ایزوتوپهای دیگر اکتینیدها با ذرات سنگینتر مانند یونهای ید یا کلسیم تولید میشوند.
جدول ایزوتوپهای مندلیفیم:
| ایزوتوپ | نیمه عمر | نوع واپاشی |
|---|---|---|
| Md-245 | 0.47 ثانیه | آلفا |
| Md-246 | 1.1 ثانیه | آلفا |
| Md-247 | 6.6 ثانیه | آلفا |
| Md-248 | 35.8 ثانیه | آلفا |
| Md-249 | 1.72 دقیقه | آلفا |
| Md-250 | 52.1 دقیقه | آلفا |
| Md-251 | 3.37 ساعت | واپاشی بتا منفی |
| Md-252 | 2.35 ساعت | واپاشی بتا منفی |
| Md-253 | 5.1 دقیقه | واپاشی بتا منفی |
| Md-254 | 28.1 دقیقه | واپاشی بتا منفی |
| Md-255 | 27.0 دقیقه | واپاشی بتا منفی |
| Md-256 | 1.01 ساعت | واپاشی بتا منفی |
| Md-257 | 5.52 ساعت | واپاشی بتا منفی |
| Md-258 | 51.5 روز | واپاشی بتا منفی |
| Md-259 | 1.83 ساعت | واپاشی بتا منفی |
| Md-260 | 31.8 ثانیه | واپاشی بتا منفی |
تاریخچه مندلیفیم: میراثی از دیمیتری ایوانوویچ مندلیف
مندلیفیم در سال 1955 توسط گروهی از دانشمندان به رهبری آلبرت گیورسو در دانشگاه کالیفرنیا، برکلی کشف شد. این دانشمندان با بمباران انیشتنیم-253 با ذرات آلفا، ایزوتوپ مندلیفیم-256 را سنتز کردند. نام مندلیفیم به پیشنهاد گیورسو و همکارانش انتخاب شد. این نام به پاس خدمات برجسته مندلیف به علم شیمی و به ویژه به دلیل ابداع جدول تناوبی، به این عنصر جدید اطلاق شد.
گروه دانشمندان آمریکایی که درگیر این کشف بودند عبارتند از گلن سیبورگ (Glenn T. Seaborg)، استنلی تامسون (Stanley Gerald Thompson)، جورج چاپین (Gregory Robert Choppin)، برنارد هاروی (Bernard G. Harvey) و آلبرت غیورسو (Albert Ghiorso).
در حدود 12 بار تکرار آزمایش، تیم دانشمندان 17 اتم مندلیفیم را تولید کردند که با روش جذب – شستشوی تبادل یونی (مندلیفیم مانند تولیوم همولوگ خاکی کمیاب رفتار می کرد) و با واپاشی جذب الکترون شناسایی شدند. با استفاده از تکنیکهای ردیاب رادیواکتیو، مندلیفیم یک حالت اکسیداسیون غالب +3 را نشان میدهد، همانطور که با موقعیت آن در سری اکتینوئید انتظار میرود. یک حالت اکسیداسیون +2 کمی پایدار نیز شناخته شده است.
پس از کشف مندلیفیم، تحقیقات گستردهای در مورد خواص و کاربردهای این عنصر انجام شد. دانشمندان با سنتز ایزوتوپهای مختلف مندلیفیم، به بررسی خواص فیزیکی و شیمیایی این عنصر پرداختند. مندلیفیم کاربردهای محدودی دارد، اما در برخی از زمینهها مانند پزشکی (در درمان برخی از انواع سرطان)، صنعت (به عنوان منبع تابش در رادیوگرافی صنعتی) و تحقیقات علمی (در مطالعه خواص عناصر ترانس اورانیوم) مفید واقع شده است.
عنصر مندلیفیم به عنوان میراثی از دیمیتری ایوانوویچ مندلیف، یادآور خدمات ارزنده این دانشمند برجسته به علم شیمی است. کشف و مطالعه این عنصر، گامی مهم در درک بهتر ساختار اتم و خواص عناصر ترانس اورانیوم محسوب میشود.
عنصر مندلیفیم به طور طبیعی در پوسته زمین یافت نمیشود. دلیل این امر، نیمه عمر بسیار کوتاه تمام ایزوتوپهای آن است. هر مندلیفیمی که در زمان شکل گیری زمین وجود داشته، تا به امروز از بین رفته است. پس مندلیفیم به طور مصنوعی در آزمایشگاه تولید میشود. روشهای مختلفی برای تولید این عنصر وجود دارد، از جمله بمباران عنصر بیسموت با یونهای آرگون و بمباران عنصر پلوتونیوم یا امریسیوم با یونهای کربن، نیتروژن یا ذرات آلفا.
جمعبندی
مندلیفیم دارای عدد اتمی 101 است و 101 پروتون در هسته یک اتم دارد. مندلیفیم یک فلز رادیواکتیو است. مندلویوم به طور طبیعی وجود ندارد. با بمباران انیشتینیم با ذرات آلفا (یون هلیوم) ساخته می شود. این اکتینوئید رنگ ناشناخته ای دارد، اما احتمالاً فلزی یا نقره ای است. این نام به نام دیمیتری مندلیف، که معمولا به عنوان پدر جدول تناوبی شناخته می شود، گرفته شده است.
پرسش و پاسخ
آیا مندلیفیم عنصری نادر است؟
مندلیفیم هرگز به طور طبیعی یافت نشده است و تنها چند میکروگرم در آزمایشگاه تولید شده است. شیمی و ظاهر آن با قطعیت مشخص نیست، اما باید مشابه سایر اکتینیدها باشد. مندلیفیم بسیار نادر است و کاربرد تجاری یا صنعتی ندارد.
آیا مندلیفیم بسیار رادیواکتیو است؟
مندلیفیم سومین عنصر سنگین اکتینید بعد از نوبلیم و لاورنسیم است. مندلیفیم یک عنصر بسیار رادیواکتیو است که نیمه عمر آن حدود 51 روز است. از طریق واپاشی آلفا، فرآیندی که در آن یک ذره آلفا از هسته ساطع می شود، به لاورنسیوم تجزیه می شود.
مندلیفیم برای چه مواردی استفاده می شود؟
در حال حاضر، هیچ کاربرد واقعی برای مندلیفیم وجود ندارد، مگر در تحقیقات. با گذشت زمان، مندلیفیم ممکن است برای اهداف فناوری و برداشت انرژی مورد استفاده قرار گیرد.
آیا مندلیفیم بی خطر است؟
مندلیفیم به طور طبیعی وجود ندارد و در پوسته زمین یافت نشده است، بنابراین دلیلی برای در نظر گرفتن خطرات سلامتی آن وجود ندارد.
فلزات, مقالات در گروه صبا | نویسنده : امید مرادی | بروزرسانی : 23 بهمن 1402