فلزاتی که در ساخت باتریها نقش دارند، امروزه اهمیت دوچندانی پیدا کردهاند زیرا با حرکت به سمت برقی شدن انواع وسایل و اشیاء، این باتریها بیشتر و بیشتر مورد استفاده قرار میگیرند. کادمیوم در باتریهای نیکل-کادمیوم و روی-کادمیوم استفاده میشود. این باتریها برای کاربردهای مختلف مانند وسایل الکترونیکی، خودروها و تجهیزات صنعتی استفاده میشوند.
کادمیوم همچنین در آلیاژهای روی مانند برنج، فولاد و آلومینیوم نیز استفاده میشود. این آلیاژها برای خواص مکانیکی و مقاومت در برابر خوردگی شناخته میشوند. بهعلاوه کادمیوم برای محافظت از فلزات دیگر در برابر خوردگی نیز استفاده میشود. این عنصر به ویژه برای محافظت از فلزات در محیطهای خورنده مانند صنایع دریایی و نفت و گاز استفاده میشود.
حال که به اهمیت این فلز پی بردید، در ادامه با صباپروفیل همراه باشید تا به بررسی کامل این عنصر بپردازیم و به سوالات مختلف پاسخ دهیم.
فهرست مطالب
عنصر و فلز کادمیوم چیست؟
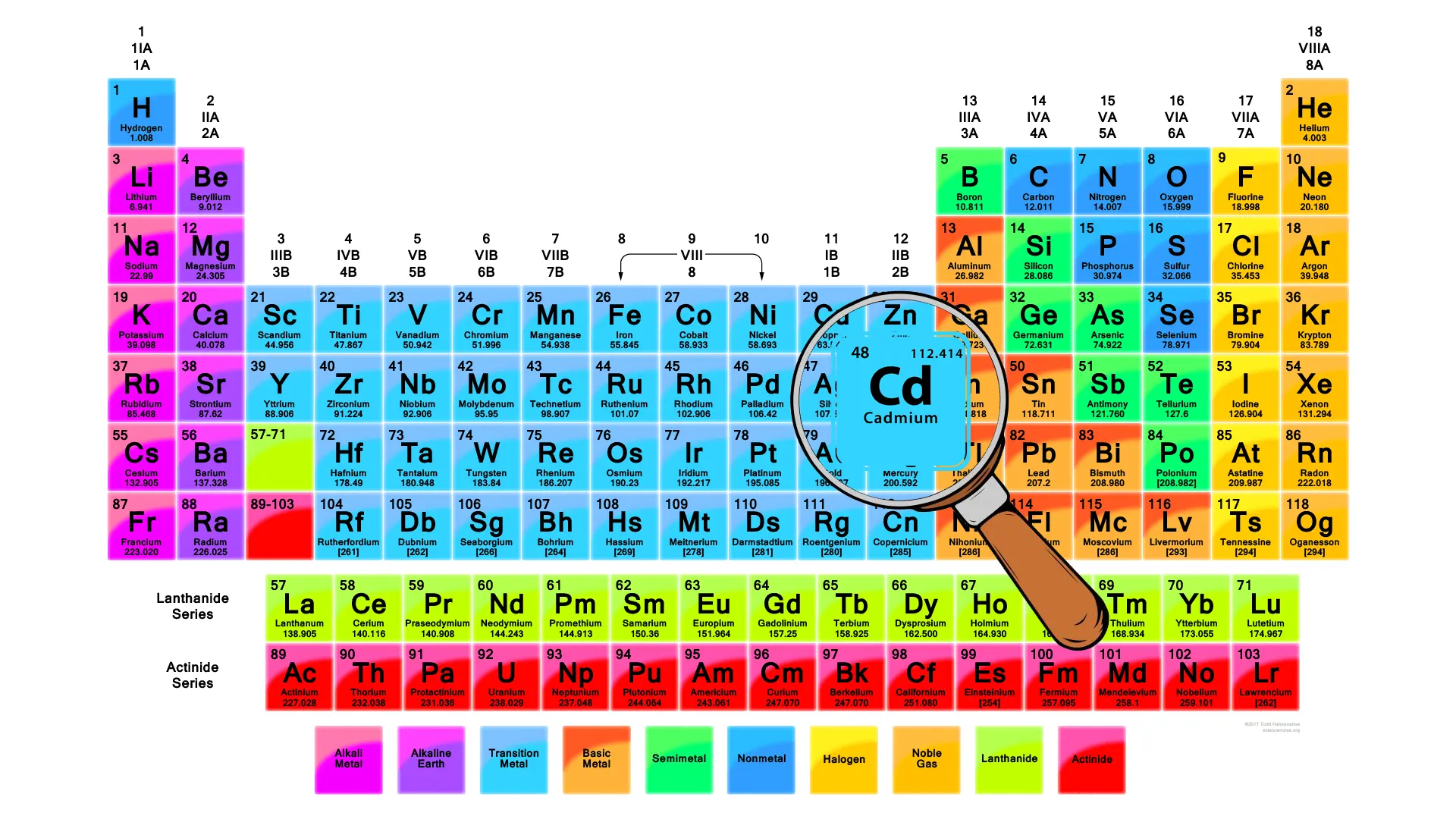
کادمیوم یک عنصر شیمیایی با نماد Cd و عدد اتمی ۴۸ است. این عنصر یک فلز نرم، سفید مایل به آبی است که از نظر شیمیایی شبیه به فلز روی است. کادمیوم در سنگ معدن روی یافت میشود و در صنعت به عنوان یک ماده اولیه برای تولید باتریها، آلیاژها، روکشها و رنگدانهها استفاده میشود.
کادمیوم یک فلز سمی است و قرار گرفتن در معرض آن میتواند منجر به مشکلات سلامتی مانند آسیب کلیه، سرطان و اختلالات باروری شود.
تاریخچه کادمیوم
کادمیوم در سال ۱۸۱۷ توسط شیمیدان آلمانی فردریش اشترومایر کشف شد. او در حال مطالعه روی بود که متوجه شد برخی از نمونههای ناخالص روی هنگام حرارت تغییر رنگ میدهند. این تغییر رنگ به دلیل وجود یک عنصر جدید بود که اشترومایر آن را کادمیوم نامید.

کادمیوم در ابتدا به عنوان یک فلز نادر و گران قیمت شناخته میشد. با این حال، در اوایل قرن بیستم، با توسعه روشهای استخراج و تولید کادمیوم، این فلز به یک ماده نسبتاً ارزان قیمت تبدیل شد.
کاربردهای کادمیوم در اوایل قرن بیستم عمدتاً در صنعت باتری بود. کادمیوم در باتریهای نیکل-کادمیوم و روی-کادمیوم استفاده میشد. در دهه ۱۹۳۰، کاربردهای جدیدی برای کادمیوم در صنعت آلیاژها، روکشها و رنگدانهها توسعه یافت.
در دهههای ۱۹۵۰ و ۱۹۶۰، استفاده از کادمیوم به طور قابل توجهی افزایش یافت. این امر به دلیل افزایش تولید باتریهای نیکل-کادمیوم و توسعه کاربردهای جدید برای کادمیوم در صنعت خودروسازی بود.
در دهه ۱۹۷۰، نگرانیهای زیستمحیطی در مورد کادمیوم افزایش یافت. کادمیوم یک فلز سمی است و میتواند به محیط زیست آسیب برساند. در نتیجه، مقرراتی برای محدود کردن استفاده از کادمیوم در برخی از کاربردها وضع شد.
در دهههای ۱۹۸۰ و ۱۹۹۰، استفاده از کادمیوم به طور قابل توجهی کاهش یافت. این امر به دلیل جایگزینی کادمیوم با مواد دیگر در برخی از کاربردها بود. با این حال، کادمیوم همچنان یکی از فلزات مهم صنعتی است و در بسیاری از محصولات استفاده میشود.
در حال حاضر، بیشترین کاربرد کادمیوم در صنعت باتری است. کادمیوم همچنین در صنعت آلیاژها، روکشها و رنگدانهها استفاده میشود.
مشخصات کادمیوم
کادمیوم به رنگ سفید نقرهای است و قابلیت جلا دادن بالایی دارد. می توان آن را به صورت ورق پهن کرد. کادمیوم در دماهای نسبتاً پایین ذوب می شود و می جوشد. بخار آن به رنگ زرد عمیق و تک اتمی است. این فلز در هوای خشک دائمی است، در هوای مرطوب با اکسید پوشیده می شود، در اثر حرارت می سوزد تا قرمز شود و به راحتی در اسیدهای معدنی محلول است.
استنشاق بخار یا گرد و غبار کادمیوم باعث مسمومیت میشود. فردریش استرومایر، شیمیدان آلمانی، این عنصر را (1817) در نمونه ای از کربنات روی کشف کرد و در همان سال، K.S.L. هرمان و جی سی اچ. رولوف کادمیوم را در نمونهای از اکسید روی یافت. هر دو ترکیب روی در حال بررسی بودند زیرا خلوص آنها به عنوان دارو مشکوک بود.
| عدد اتمی | 48 |
| وزن اتمی | 112.414 |
| نقطه ذوب (درجه سانتیگراد) | 321 |
| نقطه جوش (درجه سانتیگراد) | 765 |
| وزن مخصوص (در 20 درجه سانتیگراد) | 8.65 |
| حالت اکسیداسیون | +2 |
| پیکربندی الکترون | [Kr] 4d105s2 |
| ظرفیت گرمایی ویژه (ژول بر گرم بر درجه سانتیگراد) | ۰.۱۲۴ |
| هدایت گرمایی (وات بر متر بر درجه سانتیگراد) | ۱۲۵ |
| سختی برکول | ۱.۲ |
آبکاری کادمیوم
پوشش کادمیوم یا آبکاری کادمیوم یک فرآیند الکتروشیمیایی است که در آن یک لایه کادمیوم نازک بر روی سطح یک فلز دیگر رسوب داده میشود. این فرآیند برای محافظت از فلز زیرین در برابر خوردگی، بهبود ظاهر فلز و یا تغییر خواص آن استفاده میشود.
در فرآیند آبکاری کادمیوم، قطعهای که قرار است آبکاری شود به عنوان آند و یک کاتد فلزی مانند مس یا قلع به عنوان کاتد استفاده میشود. یک محلول الکترولیت حاوی یونهای کادمیوم بین آند و کاتد قرار میگیرد. هنگامی که جریان الکتریکی از طریق محلول الکترولیت عبور میکند، یونهای کادمیوم از کاتد به آند جذب میشوند و در آنجا به صورت فلز کادمیوم رسوب میکنند.
ضخامت لایه کادمیوم رسوب داده شده با جریان الکتریکی و زمان آبکاری کنترل میشود. به طور کلی، جریان الکتریکی بالاتر منجر به رسوب لایه کادمیوم ضخیمتر میشود. زمان آبکاری طولانیتر نیز منجر به رسوب لایه کادمیوم ضخیمتر میشود.
اکسید کادمیوم
اکسید کادمیوم (CdO) یک ترکیب شیمیایی با فرمول CdO است. این ترکیب به صورت پودر بیرنگ یا بلورهای قهوهای یا قرمز یافت میشود. اکسید کادمیوم یک ترکیب نیمه رسانا از نوع n با کافت نواری ۲.۱۸ ولت (۲.۳۱ ولت) در دمای اتاق است. اکسید کادمیوم برای اولین بار در سال ۱۸۱۷ توسط شیمیدان آلمانی، یوهان فردریش دیملر، سنتز شد.
معادن کادمیوم
کادمیوم در تعداد کمی از مواد معدنی به نام کادمییت (CdS) و گرینوکیت (CdCO3) یافت میشود. این مواد معدنی بسیار کمیاب هستند و تنها در تعداد کمی از نقاط جهان یافت میشوند. کادمیوم همچنین به مقدار کم در سایر کانیها، به ویژه سنگهای روی، یافت میشود. سنگهای روی یکی از منابع اصلی کادمیوم در جهان هستند. کادمیوم به عنوان یک محصول جانبی از استخراج و فرآوری سنگهای روی تولید میشود.
در حال حاضر، حدود 90٪ کادمیوم جهان از سنگهای روی تولید میشود. 10٪ باقیمانده از منابع دیگر مانند خاکستر زغال سنگ و پسماندهای صنعتی تولید میشود.
معادن کادمیوم در سراسر جهان یافت میشوند، اما بیشترین ذخایر کادمیوم در کشورهای زیر قرار دارد:
- چین: چین بزرگترین تولید کننده و صادر کننده کادمیوم در جهان است. ذخایر کادمیوم چین عمدتاً در استانهای شانشی، گانسو و هیلونگجیانگ یافت میشوند.
- ژاپن: ژاپن دومین تولید کننده بزرگ کادمیوم در جهان است. ذخایر کادمیوم ژاپن عمدتاً در جزیره هوکایدو یافت میشوند.
- کانادا: کانادا سومین تولید کننده بزرگ کادمیوم در جهان است. ذخایر کادمیوم کانادا عمدتاً در استانهای بریتیش کلمبیا و انتاریو یافت میشوند.
- ایالات متحده: ایالات متحده چهارمین تولید کننده بزرگ کادمیوم در جهان است. ذخایر کادمیوم ایالات متحده عمدتاً در ایالتهای آیداهو، یوتا و تگزاس یافت میشوند.
- روسیه: روسیه پنجمین تولید کننده بزرگ کادمیوم در جهان است. ذخایر کادمیوم روسیه عمدتاً در سیبری یافت میشوند.
سایر کشورهای دارای ذخایر کادمیوم عبارتند از استرالیا، شیلی، پرو، مکزیک، بولیوی، آفریقای جنوبی و جمهوری خلق چین.
ایران یکی از کشورهای دارای ذخایر کادمیوم در جهان است. ذخایر کادمیوم ایران عمدتاً در معادن روی واقع شدهاند. بر اساس اطلاعات سازمان زمینشناسی و اکتشافات معدنی ایران، بزرگترین ذخایر کادمیوم ایران در معادن زیر واقع شدهاند:
- معدن مهدیآباد (استان یزد): معدن مهدی آباد در استان یزد و در فاصله ۱۱۵ کیلومتری جنوب شرقی شهر یزد قرار دارد. این معدن با داشتن ذخایر بیش از ۲۰۰ میلیون تنی سرب و روی بزرگترین معدن در نوع خود در جهان به شمار میآید.
- معدن گوشفیل (اصفهان): این معدن نیز دارای ذخایر قابلتوجهی از سنگهای روی است که حاوی مقادیر قابلتوجهی کادمیوم نیز هستند.
- معدن ایرانکوه (اصفهان): این معدن نیز دارای ذخایر قابلتوجهی از سنگهای روی است که حاوی مقادیر قابلتوجهی کادمیوم نیز هستند. معدن ایرانکوه در استان اصفهان و در فاصله ۲۰ کیلومتری جنوب غربی شهر اصفهان قرار دارد. این معدن با داشتن ذخایر بیش از ۵ میلیون تنی سرب و روی یکی از بزرگترین معادن سرب و روی در ایران به شمار میآید.
همچنین، ذخایر کادمیوم دیگری نیز در معادن روی ایران وجود دارند که هنوز به طور کامل مورد ارزیابی قرار نگرفتهاند. در حال حاضر، استخراج کادمیوم در ایران به صورت محدود انجام میشود. کادمیوم استخراج شده از معادن ایران عمدتاً به عنوان یک محصول جانبی از استخراج و فرآوری سنگهای روی تولید میشود.
کاربردهای کادمیوم
این فلز کاربردهای مختلفی در صنایع مختلف دارد، از جمله در ساخت باتری. در ادامه بعضی از مهمترین کاربردهای کادمیوم ذکر شده است.
باتری لیتیوم کادمیوم
باتری لیتیوم کادمیوم (Li-Cd) یک نوع باتری قابل شارژ است که از لیتیوم و کادمیوم به عنوان مواد فعال خود استفاده میکند. این باتریها دارای ولتاژ بالا (3.2 ولت)، چگالی انرژی بالا (150 تا 200 واتساعت بر کیلوگرم) و چرخه عمر طولانی (1000 تا 2000 چرخه) هستند.
باتریهای لیتیوم کادمیوم برای اولین بار در دهه 1970 توسعه یافتند و به سرعت به یکی از محبوبترین انواع باتریهای قابل شارژ تبدیل شدند. این باتریها در طیف گستردهای از کاربردها از جمله تلفنهای همراه، دوربینهای دیجیتال، ابزارهای برقی و وسایل نقلیه برقی استفاده میشوند.
باتریهای لیتیوم کادمیوم دارای مزایای زیر هستند:
- ولتاژ بالا: باتریهای لیتیوم کادمیوم ولتاژ بالاتری نسبت به سایر انواع باتریهای قابل شارژ مانند باتریهای نیکل-کادمیوم و نیکل-هیدرید فلزی دارند. این امر باعث میشود که این باتریها برای کاربردهایی که به انرژی زیادی نیاز دارند مانند وسایل نقلیه برقی و ابزارهای برقی مناسب باشند.
- چگالی انرژی بالا: باتریهای لیتیوم کادمیوم چگالی انرژی بالایی دارند، به این معنی که مقدار زیادی انرژی را در یک حجم کوچک ذخیره میکنند. این امر باعث میشود که این باتریها برای کاربردهایی که به وزن کم و حجم کم نیاز دارند مانند تلفنهای همراه و دوربینهای دیجیتال مناسب باشند.
- چرخه عمر طولانی: باتریهای لیتیوم کادمیوم چرخه عمر طولانیتری نسبت به سایر انواع باتریهای قابل شارژ دارند. این امر باعث میشود که این باتریها برای کاربردهایی که به تعداد زیادی چرخه شارژ و دشارژ نیاز دارند مانند ابزارهای برقی و وسایل نقلیه برقی مناسب باشند.
باتریهای لیتیوم کادمیوم همچنین دارای معایبی نیز هستند:
- ایمنی: باتریهای لیتیوم کادمیوم میتوانند در صورت آسیب یا شارژ بیش از حد خطرناک باشند. این امر باعث میشود که این باتریها برای کاربردهایی که به ایمنی بالا نیاز دارند مانند وسایل نقلیه برقی مناسب نباشند.
- هزینه: باتریهای لیتیوم کادمیوم گرانتر از سایر انواع باتریهای قابل شارژ هستند.
در حال حاضر، باتریهای لیتیوم یونی به طور فزایندهای جایگزین باتریهای لیتیوم کادمیوم میشوند. باتریهای لیتیوم یون دارای ایمنی بالاتری هستند و هزینه کمتری دارند. با این حال، باتریهای لیتیوم کادمیوم همچنان در برخی از کاربردها مانند وسایل نقلیه برقی و ابزارهای برقی که به انرژی زیادی نیاز دارند استفاده میشوند.
باتری نیکل کادمیوم
باتری نیکل کادمیوم (NiCd) یک نوع باتری قابل شارژ است که از نیکل (III) اکسید و کادمیم به عنوان مواد فعال خود استفاده میکند. این باتریها دارای ولتاژ اسمی 1.2 ولت هستند و در طیف گستردهای از کاربردها از جمله تلفنهای همراه، دوربینهای دیجیتال، ابزارهای برقی و وسایل نقلیه برقی استفاده میشوند.
باتریهای نیکل کادمیوم برای اولین بار در دهه 1890 توسعه یافتند و به سرعت به یکی از محبوبترین انواع باتریهای قابل شارژ تبدیل شدند.
در حال حاضر، باتریهای لیتیوم-یونی به طور فزایندهای جایگزین باتریهای نیکل کادمیوم میشوند. باتریهای لیتیوم-یون دارای ایمنی بالاتری هستند، هزینه کمتری دارند و حافظه اثر ندارند. با این حال، باتریهای نیکل کادمیوم همچنان در برخی از کاربردها مانند وسایل نقلیه برقی و ابزارهای برقی که به انرژی زیادی نیاز دارند استفاده میشوند.
اثرات کادمیوم بر محیط زیست
کادمیوم یک فلز سنگین سمی است که میتواند به محیط زیست آسیب برساند. کادمیوم میتواند از طریق منابع طبیعی مانند آتشفشانها و فرسایش خاک وارد محیط زیست شود. با این حال، منبع اصلی انتشار کادمیوم در محیط زیست، فعالیتهای انسانی مانند استخراج، تولید و دفع مواد حاوی کادمیوم است. کادمیوم میتواند به محیط زیست به روشهای مختلفی وارد شود، از جمله:
- انتشار در هوا: کادمیوم میتواند از طریق احتراق سوختهای فسیلی، تولید فلزات و پردازش محصولات حاوی کادمیوم وارد هوا شود. کادمیوم موجود در هوا میتواند به خاک، آب و گیاهان برسد.
- انتشار در آب: کادمیوم میتواند از طریق فاضلاب صنعتی، زهکشی معادن و شستشوی باتریهای کادمیوم وارد آب شود. کادمیوم موجود در آب میتواند به زنجیره غذایی وارد شود.
- انتشار در خاک: کادمیوم میتواند از طریق استخراج، شستشوی باتریهای کادمیوم و دفع زبالههای حاوی کادمیوم وارد خاک شود. کادمیوم موجود در خاک میتواند توسط گیاهان جذب شود.
کادمیوم یک آلاینده زیست محیطی جدی است که میتواند به سلامت انسان و اکوسیستم آسیب برساند. قرار گرفتن در معرض کادمیوم میتواند منجر به مشکلات سلامتی زیر شود:
- آسیب کلیه: کادمیوم میتواند به سلولهای کلیه آسیب برساند و منجر به نارسایی کلیه شود.
- سرطان: قرار گرفتن در معرض کادمیوم در طولانیمدت میتواند خطر ابتلا به سرطان را افزایش دهد.
- اختلالات باروری: قرار گرفتن در معرض کادمیوم میتواند منجر به اختلالات باروری در زنان و مردان شود.
کادمیوم همچنین میتواند به اکوسیستم آسیب برساند. کادمیوم میتواند باعث کاهش رشد گیاهان و جانوران شود. همچنین میتواند باعث آلودگی آب شود و منجر به مرگ ماهیها و سایر جانوران آبزی شود.
حذف کادمیوم از آب
کادمیوم یک فلز سمی است که میتواند به محیط زیست و سلامت انسان آسیب برساند. کادمیوم میتواند از طریق منابع طبیعی مانند آتشفشانها و فرسایش خاک وارد محیط زیست شود. با این حال، منبع اصلی انتشار کادمیوم در محیط زیست، فعالیتهای انسانی مانند استخراج، تولید و دفع مواد حاوی کادمیوم است. کادمیوم میتواند به آب به روشهای مختلفی وارد شود، از جمله:
- فاضلاب صنعتی: کادمیوم میتواند از طریق فاضلاب صنعتی حاوی مواد حاوی کادمیوم وارد آب شود.
- شستشوی باتریهای کادمیوم: کادمیوم میتواند از طریق شستشوی باتریهای کادمیوم وارد آب شود.
- زهکشی معادن: کادمیوم میتواند از طریق زهکشی معادن حاوی کادمیوم وارد آب شود.
کادمیوم موجود در آب میتواند به زنجیره غذایی وارد شود و منجر به آلودگی آب آشامیدنی شود. برای کاهش اثرات کادمیوم بر محیط زیست و سلامت انسان، حذف کادمیوم از آب ضروری است. روشهای مختلفی برای حذف کادمیوم از آب وجود دارد، از جمله:
- تبادل یونی: در روش تبادل یونی، کادمیوم با یک یون دیگر مانند سدیم جایگزین میشود. این روش معمولاً برای حذف کادمیوم از آبهای صنعتی استفاده میشود.
- انعقاد و رسوب: در روش انعقاد و رسوب، کادمیوم با استفاده از مواد شیمیایی مانند کلرید کلسیم رسوب داده میشود. این روش معمولاً برای حذف کادمیوم از آبهای سطحی استفاده میشود.
- جذب سطحی: در روش جذب سطحی، کادمیوم توسط یک ماده جاذب مانند زغال فعال جذب میشود. این روش معمولاً برای حذف کادمیوم از آبهای زیرزمینی استفاده میشود.
- تصفیه با غشا: در روش تصفیه با غشا، کادمیوم با استفاده از یک غشا نیمه تراوا از آب جدا میشود. این روش معمولاً برای حذف کادمیوم از آبهای آشامیدنی استفاده میشود.
انتخاب روش مناسب برای حذف کادمیوم از آب به عوامل مختلفی مانند غلظت کادمیوم در آب، نوع آب و کاربرد آب بستگی دارد.
روش استحصال کادمیوم
در اصطلاح فنی، استحصال به فرآیندی گفته میشود که در آن یک ماده ارزشمند از یک ماده خام یا منبع طبیعی استخراج میشود. استحصال میتواند به روشهای مختلفی انجام شود، که به نوع ماده ارزشمند و منبع طبیعی آن بستگی دارد. استحصال کادمیوم به دو روش اصلی انجام میشود:
- استحصال اولیه: در این روش، کادمیوم از سنگ معدن کادمیوم به دست میآید. سنگ معدن کادمیوم معمولاً حاوی مقدار کمی کادمیوم است، بنابراین برای استخراج آن از روشهای مختلفی استفاده میشود. یکی از روشهای متداول، روش هیدرومتالورژی است که در آن سنگ معدن کادمیوم با استفاده از اسید یا باز حل میشود و کادمیوم از محلول جداسازی میشود.
- بازیافت: در این روش، کادمیوم از موادی که حاوی کادمیوم هستند، مانند باتریهای نیکل-کادمیوم، ضایعات آلیاژهای کادمیوم و رنگهای کادمیوم، بازیافت میشود. بازیافت کادمیوم مزایای مختلفی دارد، از جمله کاهش آلودگی محیط زیست، صرفهجویی در انرژی و کاهش هزینههای تولید.
روشهای مختلفی برای بازیافت کادمیوم وجود دارد. یکی از روشهای متداول، روش هیدرومتالورژی است که در آن مواد حاوی کادمیوم با استفاده از اسید یا باز حل میشوند و کادمیوم از محلول جداسازی میشود. روشهای دیگر بازیافت کادمیوم عبارتند از:
- استخراج با حلال: در این روش، مواد حاوی کادمیوم با استفاده از حلالهای خاص حل میشوند و کادمیوم از حلال جداسازی میشود.
- الکترولیز: در این روش، مواد حاوی کادمیوم در یک محلول الکترولیت قرار میگیرند و کادمیوم با استفاده از جریان الکتریکی از محلول جداسازی میشود.
روش بازیافت کادمیوم که استفاده میشود، به نوع ماده حاوی کادمیوم و مقدار کادمیوم موجود در آن بستگی دارد.
قیمت جهانی کادمیوم
قیمت جهانی کادمیوم در سالهای اخیر نوسانات زیادی داشته است. این نوسانات تحت تأثیر عوامل مختلفی از جمله تقاضا، عرضه، رشد اقتصادی، توسعه فناوریهای جدید و مقررات زیست محیطی قرار میگیرد.
در ده سال گذشته، قیمت جهانی کادمیوم روند صعودی داشته است. در سال ۲۰۱۲، قیمت کادمیوم به طور متوسط حدود ۱۰۰ دلار در هر تن بود. این قیمت در سال ۲۰۲۳ به حدود ۴۰۰ دلار در هر تن رسید. روند صعودی قیمت کادمیوم در ده سال گذشته را میتوان به دو دوره تقسیم کرد:
- دوره اول (۲۰۱۲-۲۰۲۰): در این دوره، قیمت کادمیوم به طور پیوسته افزایش یافت. این افزایش قیمت به دلیل عوامل مختلفی از جمله افزایش تقاضا برای کادمیوم در صنایع مختلف، کاهش عرضه کادمیوم و رشد اقتصادی بود.
- دوره دوم (۲۰۲۰-۲۰۲۳): در این دوره، قیمت کادمیوم روند صعودی خود را ادامه داد. این افزایش قیمت به دلیل عوامل مختلفی از جمله افزایش تقاضا برای کادمیوم در صنایع مختلف، کاهش عرضه کادمیوم و توسعه فناوریهای جدید بود.
در سال ۲۰۲۳، انتظار میرود قیمت جهانی کادمیوم همچنان افزایش یابد. این امر به دلیل افزایش استفاده از کادمیوم در صنایع مختلف، از جمله باتریهای نیکل-کادمیوم، آلیاژها، پوششها و رنگدانهها است.
پرسش و پاسخ
رنگ کادمیوم چیست؟
رنگ کادمیوم به طور کلی در سه رنگ زرد، نارنجی و قرمز موجود است. رنگ زرد کادمیوم روشن و پررنگ است و به عنوان یک رنگ پایه در رنگهای دیگر استفاده میشود. رنگ نارنجی کادمیوم نیز روشن و پررنگ است و به عنوان یک رنگ مکمل برای رنگهای دیگر استفاده میشود. رنگ قرمز کادمیوم نیز روشن و پررنگ است و به عنوان یک رنگ اصلی در رنگها استفاده میشود.
کادمیوم از طریق چه کودهایی وارد خاک میشود؟
کادمیوم یک فلز سنگین سمی است که میتواند از طریق منابع مختلفی وارد خاک شود. یکی از منابع اصلی ورود کادمیوم به خاک، کودها است. کودهایی که حاوی کادمیوم هستند عبارتند از کودهای حیوانی، کودهای شیمیایی و کودهای آلی. میزان کادمیوم موجود در کودها بسته به منبع آنها متفاوت است. به طور کلی، کودهای حیوانی حاوی مقادیر بیشتری کادمیوم نسبت به کودهای شیمیایی و آلی هستند. کادمیوم موجود در کودها میتواند به گیاهان جذب شود و از طریق زنجیره غذایی وارد بدن انسان و سایر حیوانات شود. قرار گرفتن در معرض کادمیوم میتواند باعث مشکلات سلامتی مختلفی از جمله آسیب به کلیهها، کبد و ریهها شود.
کادمیوم چه عوارضی دارد؟
کادمیوم میتواند به اندامهای مختلف بدن انسان آسیب برساند، از جمله کلیهها، کبد، ریهها، استخوانها، سیستم عصبی مرکزی و سیستم ایمنی بدن.
کادمیوم کلرید چیست؟
کادمیوم کلرید یک ترکیب شیمیایی با فرمول CdCl2 است. این ترکیب یک ترکیب جامد سفید با نقطه ذوب ۵۶۸ درجه سانتیگراد و نقطه جوش ۹۶۰ درجه سانتیگراد است. کادمیوم کلرید در آب محلول است و محلول آن اسیدی است. کادمیوم کلرید به عنوان یک ماده اولیه در تولید باتریهای نیکل-کادمیوم، آلیاژهای کادمیوم و رنگهای کادمیوم استفاده میشود. همچنین، از کادمیوم کلرید در تولید کادمیوم فلزی و سایر ترکیبات کادمیوم استفاده میشود.
نام علمی کادمیوم چیست؟
نام علمی کادمیوم Cadmium است. این نام از واژه لاتین cadmia گرفته شده است که به سنگ معدن کادمیوم اشاره دارد. کادمیوم یک فلز سنگین با عدد اتمی ۴۸ است. این فلز به رنگ سفید نقرهای است و دارای نقطه ذوب ۳۲۱ درجه سانتیگراد و نقطه جوش ۷۶۷ درجه سانتیگراد است. کادمیوم یک فلز سمی است و قرار گرفتن در معرض آن میتواند باعث مشکلات سلامتی شود.
فلزات, مقالات در گروه صبا | نویسنده : امید مرادی | بروزرسانی : 8 بهمن 1402













بعد مدتها در اخبار گوگل یه مطلب مفید دیدم این بود..ممنون
از گادمیوم در ساخت لحیم طلا و نقره جهت ساخت زیور آلات هم استفاده میشه
سلام چکیده بسیار خوبی بود ممنون . فقط یه مطلب و اصلاح کنم معدن مهدی آباد در یزد و معدن ایرانکوه هم کنار معدن گوشفیل در اصفهان واقع شده .